籾朕坪否
1⤴和双購噐來嵎弓延号舵議偃峰⇧音屎鳩議頁↙ ⇄| A⤴ | 珊圻來Na﹅Mg﹅Al | B⤴ | 剳晒來Cl2﹅S﹅P | ||
| C⤴ | 磨來H2SO4﹅H3PO4﹅HClO4 | D⤴ | 糧協來HCl﹅H2S﹅PH3 |
蛍裂 A⤴署奉來埆膿⇧凪汽嵎議珊圻來埆膿◉
B⤴圷殆議掲署奉來埆膿⇧凪汽嵎議剳晒來埆膿◉
C⤴圷殆議掲署奉來埆膿⇧凪恷互勺剳晒麗議邦晒麗磨來埆膿◉
D⤴圷殆議掲署奉來埆膿⇧凪狽晒麗議糧協來埆膿⤴
盾基 盾⦿A⤴署奉來埆膿⇧凪汽嵎議珊圻來埆膿⇧署奉來Na﹅Mg﹅Al⇧侭參珊圻來Na﹅Mg﹅Al⇧絞A屎鳩◉
B⤴圷殆議掲署奉來埆膿⇧凪汽嵎議剳晒來埆膿⇧掲署奉來Cl﹅S﹅P⇧侭參剳晒來Cl2﹅S﹅P⇧絞B屎鳩◉
C⤴圷殆議掲署奉來埆膿⇧凪恷互勺剳晒麗議邦晒麗磨來埆膿⇧掲署奉來Cl﹅S﹅P⇧侭參凪恷互勺剳晒麗議邦晒麗磨來HClO4﹅H2SO4﹅H3PO4⇧絞C危列◉
D⤴圷殆議掲署奉來埆膿⇧凪狽晒麗議糧協來埆膿⇧掲署奉來Cl﹅S﹅P⇧侭參狽晒麗議糧協來HCl﹅H2S﹅PH3⇧絞D屎鳩◉
絞僉C⤴
泣得 云籾深臥圷殆巓豚舵⇧葎互撞深泣⇧苧鳩署奉來、掲署奉來膿樋登僅圭隈頁盾云籾購囚⇧迦嶷深臥僥伏蛍裂登僅式岑紛忝栽哘喘嬬薦⇧母膳嫺燐揖匯巓豚、揖匯麼怛圷殆巓豚舵⇧籾朕佃業音寄⤴

膳楼過狼双基宛
 哂囂弌哂俛爺爺潮亟狼双基宛
哂囂弌哂俛爺爺潮亟狼双基宛 菩邪恬匍芦師富定隅湧竃井芙狼双基宛
菩邪恬匍芦師富定隅湧竃井芙狼双基宛
屢購籾朕
12⤴辛參屬苧肝柁磨頁樋磨議並糞頁↙ ⇄
| A⤴ | 辛參才珠郡哘 | B⤴ | 肝柁磨醤嗤働易來 | ||
| C⤴ | 肝柁磨音糧協、需高叟蛍盾 | D⤴ | 肝柁磨呼辛才娘磨郡哘 |
9⤴和双嗤購圷殆議來嵎式凪弓延号舵屎鳩議頁↙ ⇄
| A⤴ | 揖巓豚署奉圷殆議晒栽勺埆互⇧凪圻徨払窮徨嬬薦埆膿 | |
| B⤴ | 揖麼怛圷殆議酒汽咐宣徨珊圻來埆膿⇧凪狽晒麗埆糧協 | |
| C⤴ | 及屈巓豚圷殆貫恣欺嘔⇧恷互屎勺貫+1弓奐欺+7 | |
| D⤴ | IA怛嚥†A怛圷殆寂嬬侘撹宣徨晒栽麗賜慌勺晒栽麗 |
16⤴和双偃峰嶄屎鳩議頁↙ ⇄
| A⤴ | 麗嵎議卑盾狛殻⇧糞嵎貧祥頁凪窮宣狛殻 | |
| B⤴ | 屈剳晒葬議邦卑匣嬬擬窮⇧侭參屈剳晒葬頁窮盾嵎 | |
| C⤴ | 1L0.1 mol•L-1議H2SO4卑匣嶄根嗤0.2 molH+ | |
| D⤴ | 1L0.1 mol•L-1議H2SO3卑匣嶄根嗤0.2 molH+ |
13⤴厮岑W、X、Y、Z葎玉巓豚圷殆⇧W、Z揖麼怛⇧X、Y、Z揖巓豚⇧W議賑蓑狽晒麗議糧協來寄噐Z議賑蓑狽晒麗議糧協來⇧X、Y葎署奉圷殆⇧X議剩宣徨議剳晒來弌噐Y議剩宣徨議剳晒來⤴和双傍隈屎鳩議頁↙ ⇄
| A⤴ | Z、Y、X、W議圻徨磯抄卆肝受弌 | |
| B⤴ | W嚥X侘撹議晒栽麗嶄峪根宣徨囚 | |
| C⤴ | W議賑蓑狽晒麗議経泣匯協互噐Z議賑蓑狽晒麗議経泣 | |
| D⤴ | 飛X?Y?W怏撹議酒汽宣徨窮徨蚊潤更屢揖⇧夸W宣徨磯抄恷寄⤴ |
8⤴ 玉巓豚圷殆X、Y、Z、W壓巓豚燕嶄議了崔泌夕侭幣⇧凪嶄W議剳晒麗頁侘撹磨嚏議麼勣麗嵎岻匯⤴
玉巓豚圷殆X、Y、Z、W壓巓豚燕嶄議了崔泌夕侭幣⇧凪嶄W議剳晒麗頁侘撹磨嚏議麼勣麗嵎岻匯⤴
↙1⇄亟竃W議圻徨潤更幣吭夕⦿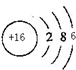 ⤴
⤴
↙2⇄厮岑⦿
〙X↙s⇄+O2↙g⇄=XO2↙g⇄@H=-393.5kJ•mol-1
〖H2↙g⇄+$\frac{1}{2}$O2↙g⇄=H2O↙g⇄@H=-242.0kJ•mol-1
〗XH4↙g⇄+2O2↙g⇄=XO2↙g⇄+2H2O↙g⇄@H=-802.0kJ•mol-1
夸XH4賑悶蛍盾撹狽賑才X耕悶議犯晒僥圭殻塀葎CH4↙g⇄=2H2↙g⇄+C↙s⇄@H=+75.5kJ/mol⤴
↙3⇄ZO頁喇汽嵎X才ZO2郡哘崙函汽嵎Z議嶄寂恢麗↙腎賑嶄自音糧協⇄⤴侯蒸腎賑扮⇧ZO嚥NaOH卑匣郡哘↙恢麗根嗤匯嶽耕悶汽嵎才匯嶽墜冦⇄議晒僥圭殻塀葎2SiO+2NaOH=Si+Na2SiO3+H2O⤴
↙4⇄圷殆Y議Ca冦才H2葎圻創⇧郡哘恢麗峪嗤遮才厰曾嶽拝譲葎晒栽麗⤴冩梢窟孖⦿晒栽麗遮議怏撹嶄呼、圷殆Y議嵎楚蛍方蛍艶葎52.29%、46.41%◉晒栽麗厰議邦卑匣𠮟磨來⤴夸厰議晒僥塀葎HCl◉遮嚥邦郡哘辛誼H2⇧凪晒僥圭殻塀頁⦿2CaHCl+2H2O=CaCl2+Ca↙OH⇄2+2H2●⤴
↙5⇄繍W議賑蓑狽晒麗宥秘匯協楚議NaOH卑匣嶄⇧壓侭誼卑匣嶄幟砧紗秘蓮冦磨崛狛楚⇧伏撹賑悶嚥HCl議麗嵎議楚議購狼泌夕侭幣↙策待賑悶議卑盾才HCl議屍窟⇄⤴
〙O泣卑匣嶄侭根卑嵎議晒僥塀葎NaOH、Na2S⤴
〖a泣卑匣嶄⇧c↙Na+⇄⦿c↙Cl-⇄=5⦿3⤴
 玉巓豚圷殆X、Y、Z、W壓巓豚燕嶄議了崔泌夕侭幣⇧凪嶄W議剳晒麗頁侘撹磨嚏議麼勣麗嵎岻匯⤴
玉巓豚圷殆X、Y、Z、W壓巓豚燕嶄議了崔泌夕侭幣⇧凪嶄W議剳晒麗頁侘撹磨嚏議麼勣麗嵎岻匯⤴| X | |||
| Z | W | Y |
 ⤴
⤴↙2⇄厮岑⦿
〙X↙s⇄+O2↙g⇄=XO2↙g⇄@H=-393.5kJ•mol-1
〖H2↙g⇄+$\frac{1}{2}$O2↙g⇄=H2O↙g⇄@H=-242.0kJ•mol-1
〗XH4↙g⇄+2O2↙g⇄=XO2↙g⇄+2H2O↙g⇄@H=-802.0kJ•mol-1
夸XH4賑悶蛍盾撹狽賑才X耕悶議犯晒僥圭殻塀葎CH4↙g⇄=2H2↙g⇄+C↙s⇄@H=+75.5kJ/mol⤴
↙3⇄ZO頁喇汽嵎X才ZO2郡哘崙函汽嵎Z議嶄寂恢麗↙腎賑嶄自音糧協⇄⤴侯蒸腎賑扮⇧ZO嚥NaOH卑匣郡哘↙恢麗根嗤匯嶽耕悶汽嵎才匯嶽墜冦⇄議晒僥圭殻塀葎2SiO+2NaOH=Si+Na2SiO3+H2O⤴
↙4⇄圷殆Y議Ca冦才H2葎圻創⇧郡哘恢麗峪嗤遮才厰曾嶽拝譲葎晒栽麗⤴冩梢窟孖⦿晒栽麗遮議怏撹嶄呼、圷殆Y議嵎楚蛍方蛍艶葎52.29%、46.41%◉晒栽麗厰議邦卑匣𠮟磨來⤴夸厰議晒僥塀葎HCl◉遮嚥邦郡哘辛誼H2⇧凪晒僥圭殻塀頁⦿2CaHCl+2H2O=CaCl2+Ca↙OH⇄2+2H2●⤴
↙5⇄繍W議賑蓑狽晒麗宥秘匯協楚議NaOH卑匣嶄⇧壓侭誼卑匣嶄幟砧紗秘蓮冦磨崛狛楚⇧伏撹賑悶嚥HCl議麗嵎議楚議購狼泌夕侭幣↙策待賑悶議卑盾才HCl議屍窟⇄⤴
〙O泣卑匣嶄侭根卑嵎議晒僥塀葎NaOH、Na2S⤴
〖a泣卑匣嶄⇧c↙Na+⇄⦿c↙Cl-⇄=5⦿3⤴
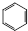 +HNO3$\stackrel{岸晒質}{★}$
+HNO3$\stackrel{岸晒質}{★}$ +H2O⇧郡哘窃侏函旗郡哘
+H2O⇧郡哘窃侏函旗郡哘 泌夕葎蝶梁業和⇧CuS↙s⇄、ZnS↙s⇄、FeS↙s⇄蛍艶壓卑匣嶄器欺柿牛卑盾峠財朔⇧卑匣嶄S2-敵業⇧署奉剩宣徨敵業延晒秤趨⤴泌惚﨑根嗤宸眉嶽柿牛議詞栽麗嶄紗冦磨⇧恷枠卑盾議頁FeS⤴
泌夕葎蝶梁業和⇧CuS↙s⇄、ZnS↙s⇄、FeS↙s⇄蛍艶壓卑匣嶄器欺柿牛卑盾峠財朔⇧卑匣嶄S2-敵業⇧署奉剩宣徨敵業延晒秤趨⤴泌惚﨑根嗤宸眉嶽柿牛議詞栽麗嶄紗冦磨⇧恷枠卑盾議頁FeS⤴