题目内容
本题共2个小题,请按要求作答.
(1)根据下列各组物质,回答问题(均填选项号):
A.O2与O3 B. 12C与13C C.正丁烷和异丁烷 D.
E.甲烷和庚烷 F.D与T G.金刚石与“足球烯”C60 H.16O、17O和18O
①互为同位素的是 ;
②互为同素异形体的是 ;
③属于同系物的是 ;
④互为同分异构体的是 ;
⑤属于同一物质的是 .
(2)用Cl2生产某些含氯有机物时会产生副产物HCl.利用下列反应,可实现氯的循环利用.
反应:4HCl+O2═2Cl2+2H2O
已知:该反应中,4mol HCl被氧化,放出115.6kJ的热量.

①H2O的电子式为 .
②该反应中反应物的总能量 生成物的总能量.(填“大于、小于或等于”)
③断开1mol H-O 键与断开 1mol H-Cl 键所需能量相差约为 kJ,H2O中H-O键比HCl中H-Cl键 (填“强”或“弱”).
(1)根据下列各组物质,回答问题(均填选项号):
A.O2与O3 B. 12C与13C C.正丁烷和异丁烷 D.

E.甲烷和庚烷 F.D与T G.金刚石与“足球烯”C60 H.16O、17O和18O
①互为同位素的是
②互为同素异形体的是
③属于同系物的是
④互为同分异构体的是
⑤属于同一物质的是
(2)用Cl2生产某些含氯有机物时会产生副产物HCl.利用下列反应,可实现氯的循环利用.
反应:4HCl+O2═2Cl2+2H2O
已知:该反应中,4mol HCl被氧化,放出115.6kJ的热量.

①H2O的电子式为
②该反应中反应物的总能量
③断开1mol H-O 键与断开 1mol H-Cl 键所需能量相差约为
考点:同位素及其应用,同素异形体,反应热和焓变,芳香烃、烃基和同系物,同分异构现象和同分异构体
专题:化学反应中的能量变化,原子组成与结构专题
分析:(1)具有相同质子数、不同中子数的原子为同位素;
具有相同分子式、不同结构的有机物互为同分异构体;
结构相似,分子组成相差n个CH2原子团的有机物互为同系物;
同种元素的不同单质,互为同素异形体;
分子式相同、结构相同的物质为同一种物质,以此来解答;
(2)①水是共价化合物依据电子式书写方法写出电子式;
②根据放热反应中,反应物的总能量大于生成物的总能量,反之小于生成物的总能量;
③依据反应A中,4mol HCl被氧化,放出115.6kJ的热量,焓变=反应物断键吸收热量-生成物形成化学键放出热量计算.
具有相同分子式、不同结构的有机物互为同分异构体;
结构相似,分子组成相差n个CH2原子团的有机物互为同系物;
同种元素的不同单质,互为同素异形体;
分子式相同、结构相同的物质为同一种物质,以此来解答;
(2)①水是共价化合物依据电子式书写方法写出电子式;
②根据放热反应中,反应物的总能量大于生成物的总能量,反之小于生成物的总能量;
③依据反应A中,4mol HCl被氧化,放出115.6kJ的热量,焓变=反应物断键吸收热量-生成物形成化学键放出热量计算.
解答:
解:(1)A.O2与O3为氧元素的不同单质,互为同素异形体;
B.12C与13C的质子数相同、中子数不同,二者为同位素;
C.正丁烷和异丁烷具有相同分子式、不同结构,互为同分异构体;
D. 分子式相同、结构相同的物质,则为同一种物质,
分子式相同、结构相同的物质,则为同一种物质,
E.甲烷和庚烷结构相似,分子组成相差7个CH2原子团,互为同系物;
F.D与T的质子数相同、中子数不同,二者为同位素;
G.金刚石与“足球烯”C60 为碳元素的不同单质,互为同素异形体;
H.16O、17O和18O的质子数相同、中子数不同,二者为同位素;
故答案为:①BFH;②AG;③E;④C;⑤D;
(2)①水是共价化合物,氧原子和两个氢原子形成两个共价键,电子式为: ,故答案为:
,故答案为: ;
;
②依据题目可知,该反应放热,反应物的总能量大于生成物的总能量,故答案为:>;
③焓变=反应物断键吸收热量-生成物形成化学键放出热量,4HCl(g)+O2(g)?2Cl2(g)+2H2O(g)△H=-115.6 KJ/mol,
4×E(H-Cl)+498-[243×2+4×E(H-O)]=-115.6,得到4×E(H-O)-4×E(H-Cl)=498-486+115.6=127.6,E(H-O)-E(H-Cl)=31.9,H2O中H-O键比HCl中H-Cl键强,
故答案为:31.9;强.
B.12C与13C的质子数相同、中子数不同,二者为同位素;
C.正丁烷和异丁烷具有相同分子式、不同结构,互为同分异构体;
D.
 分子式相同、结构相同的物质,则为同一种物质,
分子式相同、结构相同的物质,则为同一种物质,E.甲烷和庚烷结构相似,分子组成相差7个CH2原子团,互为同系物;
F.D与T的质子数相同、中子数不同,二者为同位素;
G.金刚石与“足球烯”C60 为碳元素的不同单质,互为同素异形体;
H.16O、17O和18O的质子数相同、中子数不同,二者为同位素;
故答案为:①BFH;②AG;③E;④C;⑤D;
(2)①水是共价化合物,氧原子和两个氢原子形成两个共价键,电子式为:
 ,故答案为:
,故答案为: ;
;②依据题目可知,该反应放热,反应物的总能量大于生成物的总能量,故答案为:>;
③焓变=反应物断键吸收热量-生成物形成化学键放出热量,4HCl(g)+O2(g)?2Cl2(g)+2H2O(g)△H=-115.6 KJ/mol,
4×E(H-Cl)+498-[243×2+4×E(H-O)]=-115.6,得到4×E(H-O)-4×E(H-Cl)=498-486+115.6=127.6,E(H-O)-E(H-Cl)=31.9,H2O中H-O键比HCl中H-Cl键强,
故答案为:31.9;强.
点评:本题是道综合题,涉及知识点较多,五同、电子式的书写、热化学方程式书写,化学键键能和焓变关系计算,图象分析判断,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
在3NO2(g)+H2O(l)?2HNO3(aq)+NO(g)△H<0反应达到平衡后,改变下列条件,可使HNO3浓度增大的是( )
| A、升温 |
| B、减压 |
| C、加水 |
| D、通入O2 |
除去括号内杂质所用试剂和方法不正确的是( )
| A、Cu(Fe)--加盐酸,过滤 |
| B、乙醇(水)--加生石灰,蒸馏 |
| C、KNO3溶液(KCl)--降温结晶,过滤 |
| D、CO2(HCl)--饱和NaOH溶液,洗气 |
下列关于胶体的叙述中正确的是( )
| A、液溶胶是一种液态混合物属于分散系的一种 |
| B、直径介于1 nm~10 nm之间的微粒称为胶体 |
| C、胶体的本质特征是发生丁达尔效应 |
| D、用过滤器可以将胶体和溶液分开 |
 人们应用原电池原理制作了多种电池以满足不同的需要.在现代生活、生产和科学技术发展中,电池发挥着越来越重要的作用,如在宇宙飞船、人造卫星、空间电视转播站、飞机、轮船、电脑、收音机、照相机、电子手表、心脏起搏器等,都离不开各式各样的电池,同时废弃的电池随便丢弃也会对环境造成污染.请根据题中提供的信息,回答下列问题:
人们应用原电池原理制作了多种电池以满足不同的需要.在现代生活、生产和科学技术发展中,电池发挥着越来越重要的作用,如在宇宙飞船、人造卫星、空间电视转播站、飞机、轮船、电脑、收音机、照相机、电子手表、心脏起搏器等,都离不开各式各样的电池,同时废弃的电池随便丢弃也会对环境造成污染.请根据题中提供的信息,回答下列问题: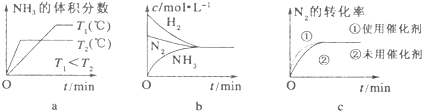
 一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):
一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):