题目内容
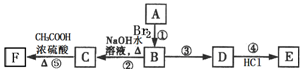
17.硼与铝的性质相似,能与氧气、氢氧化钠溶液等物质反应.硼与氯气反应生成三氯化 硼(BCl3),生成的三氯化硼遇水水解产生白雾(BCl3+3H2O=H3BO3+3HCl)(已知:BCl3的熔点为-107.3℃,沸点为12.5℃),且三氯化硼用于制取乙硼烷(B2H6).某兴趣小组设计如图所示装置制备三氯化硼.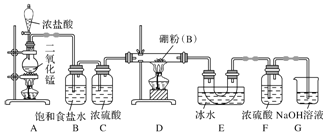
回答下列问题:
(1)盛浓盐酸的装置名称为分液漏斗.
(2)装置E的作用是冷却和收集三氯化硼
(3)装置D中发生反应的化学方程式为2B+3Cl2$\frac{\underline{\;\;△\;\;}}{\;}$2BCl3.
(4)装置F的作用是防止水蒸气进入装置E,可以用一个盛装碱石灰(填试剂名称)的干燥管代替装置F和G,使实验更简便.
(5)为了顺利完成实验,点燃酒精灯的正确操作是A(填字母),其理由是先用Cl2排尽装置中的空气,避免氧气和硼粉反应.
a.先点燃A处酒精灯,后点燃D处酒精灯
b.先点燃D处酒精灯,后点燃A处酒精灯
c.同时点燃A、D两处酒精灯.
分析 A装置制备氯气,制备的氯气中含有HCl、水蒸气,B装置吸收HCl,C装置干燥氯气,D装置中氯气与硼反应生成BCl3,E装置冷却和收集三氯化硼,三氯化硼遇水水解,F装置防止水蒸气加入E中,氯气有毒,直接排放会污染空气,G装置吸收氯气,据此分析作答.
解答 解:A装置制备氯气,制备的氯气中含有HCl、水蒸气,B装置吸收HCl,C装置干燥氯气,D装置中氯气与硼反应生成BCl3,E装置冷却和收集三氯化硼,三氯化硼遇水水解,F装置防止水蒸气加入E中,氯气有毒,直接排放会污染空气,G装置吸收氯气.
(1)由仪器结构可知盛装浓盐酸的仪器为分液漏斗;
故答案为:分液漏斗;
(2)E中冰水冷却便于收集三氯化硼;
故答案为:冷却和收集三氯化硼;
(3)D中氯气与硼在加热条件下生成三氯化硼,反应方程式为:2B+3Cl2$\frac{\underline{\;\;△\;\;}}{\;}$2BCl3;
故答案为:2B+3Cl2$\frac{\underline{\;\;△\;\;}}{\;}$2BCl3;
(4)由于三氯化硼遇水水解,F装置防止水蒸气加入装置E中,可以用一个盛装碱石灰的干燥管代替装置F和G;
故答案为:防止水蒸气进入装置E;碱石灰;
(5)根据题中信息可知:硼能与氧气反应,故应先通氯气排除装置中的空气,防止硼与空气中的氧气反应,所以在加热制备三氯化硼,故先点燃A处酒精灯,后点燃D处酒精灯;
故答案为:A;先用Cl2排尽装置中的空气,避免氧气和硼粉反应.
点评 本题考查物质制备实验,侧重于学生的分析能力和实验能力的考查,题目涉及制备气体、净化气体、干燥气体和尾气处理,明确原理是解题关键,注意题目信息的应用,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.下列现象与胶体知识无关的是( )
| A. | 胶体中分散质粒子的直径大于溶液中分散质的粒子直径 | |
| B. | 向饱和的氯化铁溶液中加入氢氧化钠溶液得到红褐色沉淀 | |
| C. | 明矾【KAl(SO4)2•12H2O】可以做净水剂 | |
| D. | 氢氧化铁溶胶、稀豆浆、云雾等均具有丁达尔现象 |
9.常温下,下列各组离子一定能在指定溶液中大量共存的是( )
| A. | 中性溶液中:K+、Fe3+、SO42-、Cl- | |
| B. | 水电离的c(H+)=1×10-13mol/L的溶液中:K+、Na+、[Al(OH)4]-、CO32- | |
| C. | 与Al反应能放出H2的溶液中:Fe2+、Na+、NO3-、SO42- | |
| D. | $\frac{{K}_{W}}{c({H}^{+})}$=1×10-13mol/L的溶液中:K+、Cu2+、Cl-、NO3- |
7.NA为阿伏加德罗常数,下列说的是( )
| A. | 2.24LCO2中含0.3NA原子 | |
| B. | 0.3molNH4NO3固体中含0.3NANH4+ | |
| C. | 5.6g铁粉完全反应一定失去0.3NA电子 | |
| D. | 25℃,0.1NAHCl气体溶于1L水,溶液pH=1 |

 工业纯碱中常常含有NaCl、Na2SO4等杂质.为测定某工业纯碱的纯度,设计了如右图实验装置.依据实验设计,请回答:
工业纯碱中常常含有NaCl、Na2SO4等杂质.为测定某工业纯碱的纯度,设计了如右图实验装置.依据实验设计,请回答: