题目内容
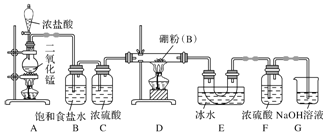
8.ICl是一种红棕色液体或黑色结晶,沸点97.4°C,不溶于水,可溶于乙醇和乙酸.用ICl间接测定油脂中碘值的主要步骤如下:步骤1.制备ICl:在三口烧瓶中加入精制的单质碘和盐酸,控制温度约50℃,在不断搅拌下逐滴加入计量的NaClO3溶液,分离提纯后得纯净的ICl.
步骤2.配制韦氏试剂:称取16.25gICl与冰醋酸配成1000mL韦氏试剂.
步骤3.测定碘值:称取0.4000g某品牌调和油加入碘量瓶中(带玻璃塞的锥形瓶),加入20mL三氯甲烷轻轻摇动使其溶解,再加入韦氏试剂25.00mL,充分摇匀,塞紧瓶塞置暗处约30min(R1CH=CHR2+ICl→R1CHI-CHClR2).继续加入10mL20%KI溶液(KI+ICl=KCl+I2)、100mL蒸馏水,用淀粉作指示剂,用0.1000mol•L-1Na2S2O3溶液滴定(I2+2Na2S2O3=2NaI+Na2S4O6),滴定到终点时消耗Na2S2O3溶液24.00mL.
(1)步骤1温度不宜超过50℃,其原因是防止碘升华和ICl挥发;制备ICl反应的化学方程式为3I2+6HCl+NaClO3=6ICl+NaCl+3H2O.
(2)步骤2配制韦氏试剂需要的玻璃仪器除烧杯、量筒及玻璃棒外,还需要1000mL容量瓶和胶头滴管(填仪器名称).
(3)油脂的碘值是指每100g油脂与单质碘发生加成反应时所能吸收的碘的质量(单位g/100g油脂),根据以上实验数据计算该调和油的碘值(写出计算过程).
分析 (1)碘单质易升华,ICl挥发,温度不宜过高;碘单质与氯酸钠在酸性条件下反应生成ICl,配平可得;
(2)配制1000mL溶液需要的玻璃仪器除烧杯、量筒及玻璃棒1000mL容量瓶和胶头滴管;
(3)已知加入的ICl的总物质的量,根据消耗的Na2S2O3溶液计算过量的ICl的物质的量,则可得油脂消耗的ICl的物质的量,由此计算该调和油的碘值.
解答 解:(1)防止碘升华和ICl挥发,步骤1温度不宜超过50℃;碘单质与氯酸钠在酸性条件下反应生成ICl,碘元素化合价升高,氯酸钾中氯元素化合价降低到-1价,结合盐酸,反应为:3I2+6HCl+NaClO3=6ICl+NaCl+3H2O;
故答案为:防止碘升华和ICl挥发;3I2+6HCl+NaClO3=6ICl+NaCl+3H2O;
(2)配制1000mL溶液需要的玻璃仪器除烧杯、量筒及玻璃棒1000mL容量瓶和胶头滴管;
故答案为:1000mL容量瓶和胶头滴管;
(3)起始加入的ICl的物质的量为:$\frac{16.25g}{162.5g/mol}×\frac{25.00mL}{1000mL}$=2.500×10-3mol
滴定消耗n(Na2S2O3)=0.1000mol•L-1×24.00mL×10-3L•mL-1=2.400×10-3mol
过量的n(ICl)=n(I2)=$\frac{1}{2}$n(Na2S2O3)=1.200×10-3mol
油脂消耗的n(ICl)=2.500×10-3m2ol-1.200×10-3mol=1.300×10-3mol
碘值为:1.300×10-3mol×254g•mol-1×$\frac{100g}{0.4000g}$=82.6g/100g油脂
答:该调和油的碘值82.6g/100g油脂.
点评 本题考查了实验条件的控制,仪器的选择,有关计算,题目难度中等,注意对基础知识的掌握和计算.

| A. | 正极反应式为:O2+4e-+2H2O=4OH- | |
| B. | 工作一段时间后,电解液中硫酸的物质的量浓度不变 | |
| C. | 通氢气的电极上发生还原反应 | |
| D. | 溶液中氢离子流向通氧气的电极 |
| 阳极 | 阴极 | 溶液甲 | 物质乙 | |
| A | Pt | Pt | NaOH | NaOH固体 |
| B | Pt | Pt | H2SO4 | H2O |
| C | Pt | Pt | NaCl | NaOH |
| D | 粗铜 | 精铜 | CuSO4 | Cu(OH)2 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 95℃纯水的pH<7,说明加热可导致水呈酸性 | |
| B. | pH=3的醋酸溶液稀释至10倍后pH=4 | |
| C. | 0.2 mol/L的盐酸与0.1 mol/L的盐酸等体积混合后pH=1.5 | |
| D. | 若向氨水中加入等浓度稀盐酸至溶液正好呈中性,则所用稀盐酸的体积一定小于氨水的体积 |
 .
.