题目内容
20.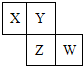 X、Y、Z、W均为短周期元素,它们在周期表中位置如图所示,若Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在周期表中位置如图所示,若Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是( )| A. | 非金属性:W>Z>Y | |
| B. | 最高价氧化物对应水化物的酸性:Z>W>X | |
| C. | 气态氢化物的稳定性:X>Y>Z | |
| D. | 最高正化合价:W>Z>X |
分析 X、Y、Z、W均为短周期元素,Y原子的最外层电子数是内层电子数的3倍,则Y原子有2个电子层,所以Y为氧元素,根据X、Y、Z、W在周期表中相对位置可知,X为氮元素,Z为硫元素,W为氯元素.结合元素性质的递变规律分析解答.
解答 解:A.同主族元素从上到下元素的非金属性逐渐减小,Y>Z,故A错误;
B.同周期元素从左到右元素的非金属性逐渐增强,非金属性Z<W,则最高价氧化物对应水化物的酸性Z<W,故B错误;
C.同周期元素从左到右元素的非金属性逐渐增强,非金属性X<Y,则气态氢化物的稳定性:X<Y,故C错误;
D.同周期元素从左到右核外电子数逐渐增多,最高化合价逐渐增大,分别为+7、+6、+5,故D正确.
故选D.
点评 本题考查元素周期表与元素周期律,难度不大,注意掌握元素周期律,理解同主族、同周期元素性质的递变规律.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
10.130mol浓度为3mol•L-1是盐酸跟过量的锌片反应,为加快反应速率,又不影响生成氢气的总量,可采用的方法是( )
| A. | 加入适量的6mol•L-1的盐酸 | B. | 加入数滴氯化铜溶液 | ||
| C. | 加入数滴硝酸铜溶液 | D. | 加入适量的氯化钠溶液 |
11.全部由第三周期元素形成的化合物是( )
| A. | HF | B. | NO | C. | Na2S | D. | MgF2 |
5.下列有关能源的说法不正确的是( )
| A. | 人类利用能源的三个阶段分别是:柴草时期、化石能源时期、多能源结构时期 | |
| B. | 人类使用沼气是对化学能的充分利用 | |
| C. | 海底有大量的天然气水合物-“可燃冰”,它是一种比较洁净的能源 | |
| D. | 生物质能主要指用树木、庄稼、草类等植物直接或间接提供的能量,它是不可再生的能源 |
9.用NA表示阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 用石墨作电极电解饱和食盐水时,若阴极得到2NA个电子,则阳极产生22.4L气体 | |
| B. | 常温常压下,Na2O2与足量H2O反应,共生成0.2mol O2,转移的电子数目是0.8NA | |
| C. | 1L 1mol/L的K2CO3溶液中离子总数小于3NA | |
| D. | 室温下,42.0g 乙烯和丙烯的混合气体中含有的碳原子数为3NA |
20.机物A的结构如图所示,下列说法正确的是( )
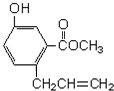

| A. | 一定条件下和浓溴水反应时,1mol A能消耗3molBr2 | |
| B. | 一定条件下,1mol A能和5mol氢气发生加成反应 | |
| C. | 一定条件下,1mol A能与3molNaOH反应 | |
| D. | A能与碳酸氢钠溶液反应 |