题目内容
8.在标准状况下,用将一充满HCl和氧气混合气体的集气瓶倒放于盛有足量水的水槽中,水面上升至集气瓶容积的$\frac{3}{5}$就停止了,若假设HCl全部留在集气瓶中,则集气瓶内所得溶液HCl的物质的量浓度为$\frac{1}{22.4}$mol/L.分析 HCl极易溶于水,氧气不易溶于水,所以水面上升的体积就是HCl的体积,设容器体积为VL,水面上升至集气瓶容积的$\frac{3}{5}$就停止了,则氯化氢体积=$\frac{3}{5}$VL,溶液体积为$\frac{3}{5}$VL,n(HCl)=$\frac{\frac{3}{5}VL}{22.4L/mol}$=$\frac{\frac{3V}{5}}{22.4}$mol,根据c=$\frac{n}{V}$计算盐酸浓度.
解答 解:HCl极易溶于水,氧气不易溶于水,所以水面上升的体积就是HCl的体积,设容器体积为VL,水面上升至集气瓶容积的$\frac{3}{5}$就停止了,则氯化氢体积=$\frac{3}{5}$VL,溶液体积为$\frac{3}{5}$VL,n(HCl)=$\frac{\frac{3}{5}VL}{22.4L/mol}$=$\frac{\frac{3V}{5}}{22.4}$mol,则盐酸物质的量浓度=$\frac{\frac{\frac{3V}{5}}{22.4}mol}{\frac{3}{5}VL}$=$\frac{1}{22.4}$mol/L,
故答案为:$\frac{1}{22.4}$mol/L.
点评 本题考查物质的量的有关计算,为高频考点,明确水上升体积与HCl气体体积关系是解本题关键,熟悉物质的量公式中各个物理量的关系,题目难度不大.

练习册系列答案
相关题目
19.化学与生产、生活、社会密切相关,下列叙述错误的是( )
| A. | 食品保鲜膜、一次性食品袋的主要成分是聚氯乙烯 | |
| B. | 工业燃煤中加入适量的生石灰能有效减少二氧化硫的排放量 | |
| C. | 若同时使用硫酸亚铁和氯气处理水,能达到消毒杀菌和除去悬浮杂质的目的 | |
| D. | 航天服的主要成分是碳化硅、陶瓷和碳纤维,它们都属于无机非金属材料 |
16.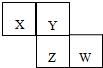 X、Y、Z、W为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是( )
X、Y、Z、W为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是( )
 X、Y、Z、W为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是( )
X、Y、Z、W为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是( )| A. | 原子半径:W>Z>X | |
| B. | 非金属性:Z>Y | |
| C. | 最高化合价:Z>X | |
| D. | 最高价氧化物对应水化物的酸性:W>Z |
13.下列关于电解质溶液说法正确的是( )
| A. | NaCl溶液与CH3COOHNH4溶液均显中性,两溶液中水的电离程度相同 | |
| B. | CH3COONa溶液加水稀释:$\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$减小 | |
| C. | 在NaHSO3溶液中,c(H+)+c(H2SO3)=c(OH-)+c(SO32-) | |
| D. | 含有AgCl和AgBr固体的悬浊液:c(Ag+)>c(Cl-)=c(Br-) |
20.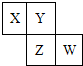 X、Y、Z、W均为短周期元素,它们在周期表中位置如图所示,若Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在周期表中位置如图所示,若Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是( )
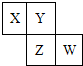 X、Y、Z、W均为短周期元素,它们在周期表中位置如图所示,若Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在周期表中位置如图所示,若Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是( )| A. | 非金属性:W>Z>Y | |
| B. | 最高价氧化物对应水化物的酸性:Z>W>X | |
| C. | 气态氢化物的稳定性:X>Y>Z | |
| D. | 最高正化合价:W>Z>X |
8.某学生在做同主族元素性质递变规律的实验时,自己设计了一套实验方案,并记录了有关的实验现象.现在请你帮助该学生整理并完成实验报告.
(1)实验目的:探究同一主族元素性质的递变规律.
(2)实验用品:
仪器:试管、胶头滴管.
药品:氯水、溴水、溴化钠溶液、碘化钾溶液、四氯化碳.
(3)实验内容(在下表横线中填写相关内容):
(4)实验结论:同一主族,自上而下,元素的非金属性依次减弱.
(5)问题和讨论:
①上述两个实验中发生反应的离子方程式分别为Cl2+2Br-═2Cl-+Br2、Br2+2I-═2Br-+I2.
②由于F2过于活泼,所以很难设计出一个简单的实验来验证其氧化性的强弱.试列举两项事实说明氟的非金属性比氯强:F2在冷暗处就可以与H2剧烈反应而爆炸,而Cl2与H2要在光照或点燃时才反应、HF比HCl更稳定.
(1)实验目的:探究同一主族元素性质的递变规律.
(2)实验用品:
仪器:试管、胶头滴管.
药品:氯水、溴水、溴化钠溶液、碘化钾溶液、四氯化碳.
(3)实验内容(在下表横线中填写相关内容):
| 序号 | 实验方案 | 实验现象 |
| ① | 向盛有少量溴化钠溶液的试管中滴加少量新制的氯水,振荡,再注入少量四氯化碳,振荡后静置 | 液体分为两层,下层呈橙色 |
| ② | 向盛有少量碘化钾溶液的试管中滴加少量溴水,振荡,再注入少量四氯化碳,振荡后静置 | 液体分为两层,下层呈紫色 |
(5)问题和讨论:
①上述两个实验中发生反应的离子方程式分别为Cl2+2Br-═2Cl-+Br2、Br2+2I-═2Br-+I2.
②由于F2过于活泼,所以很难设计出一个简单的实验来验证其氧化性的强弱.试列举两项事实说明氟的非金属性比氯强:F2在冷暗处就可以与H2剧烈反应而爆炸,而Cl2与H2要在光照或点燃时才反应、HF比HCl更稳定.
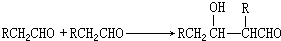
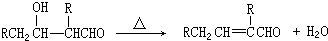

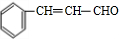 ;
;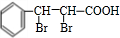 +2NaOH$→_{△}^{乙醇}$
+2NaOH$→_{△}^{乙醇}$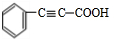 +2NaBr+2H2O
+2NaBr+2H2O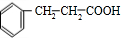 +
+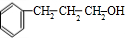 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$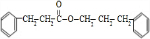 +H2O.
+H2O.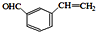 、
、 、
、
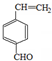 .
.