题目内容
16.下表中的数据是破坏1mol物质中的化学键所消耗的能量(KJ)| 物质 | Cl2 | Br2 | I2 | HCl | HBr | HI | H2 |
| 能量(kJ) | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
| A. | 放出248 kJ 热量 | B. | 吸收248 kJ 热量 | C. | 放出183kJ 热量 | D. | 吸收183 kJ 热量 |
分析 根据反应热等于反应物的总键能减去生成物的总键,进行分析求解.
解答 解:1molH2与1molCl2反应生成2molHCl的能量变化,△H=436+243-2×432=-185kJ/mol,所以1molH2与1molCl2反应生成2molHCl放出热量为:185kJ,故选C.
点评 本题考查化学方程式中热量的变化,特别考查了△H=反应物的键能和-生成物的键能和的运用.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
16.能够快速、微量、精确地测定相对分子质量的物理方法是( )
| A. | 红外光谱 | B. | 质谱 | C. | 核磁共振谱 | D. | 紫外光谱 |
8.将下列物质熔化:氢氧化钠、二氧化硅、氧化钙、冰,需要克服的微粒间的相互作用 ①共价键 ②离子键 ③分子间作用力、氢键,正确的顺序是( )
| A. | .①②②③ | B. | ②③②① | C. | ②①②③ | D. | ①①②③ |
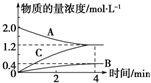 如图,曲线表示在800℃时和某反应有关的物质A、B、C的物质的量浓度从开始反应至4min时的变化图象,试回答:
如图,曲线表示在800℃时和某反应有关的物质A、B、C的物质的量浓度从开始反应至4min时的变化图象,试回答: ;
;