题目内容
8.将下列物质熔化:氢氧化钠、二氧化硅、氧化钙、冰,需要克服的微粒间的相互作用 ①共价键 ②离子键 ③分子间作用力、氢键,正确的顺序是( )| A. | .①②②③ | B. | ②③②① | C. | ②①②③ | D. | ①①②③ |
分析 离子晶体中含有离子键,原子晶体中含有共价键,分子晶体中含有分子间作用力(可能含有氢键),根据晶体类型确定熔化晶体时克服的微粒间作用力.
解答 解:NaOH和CaO属于离子晶体,熔化时需要克服的是离子键;
SiO2属于原子晶体,熔化时需要克服的是共价键;
水属于分子晶体,熔化时需要克服的是分子间作用力,水分子间还形成氢键,故还破坏了氢键;
故选C.
点评 本题考查了晶体的类型,明确晶体的构成微粒是解本题关键,难度不大.

练习册系列答案
相关题目
8. 常温下,向20ml某浓度的硫酸溶液中滴入0.1mol•l-1氨水,溶液中水电离的氢离子浓度随加入氨水的体积变化如图.下列分析正确的是( )
常温下,向20ml某浓度的硫酸溶液中滴入0.1mol•l-1氨水,溶液中水电离的氢离子浓度随加入氨水的体积变化如图.下列分析正确的是( )
 常温下,向20ml某浓度的硫酸溶液中滴入0.1mol•l-1氨水,溶液中水电离的氢离子浓度随加入氨水的体积变化如图.下列分析正确的是( )
常温下,向20ml某浓度的硫酸溶液中滴入0.1mol•l-1氨水,溶液中水电离的氢离子浓度随加入氨水的体积变化如图.下列分析正确的是( )| A. | V=40 | |
| B. | C点所示溶液中:c(H+)-c(OH-)═2c(NH3•H2O) | |
| C. | d点所示溶液中:c(NH4+)═2c(SO42-) | |
| D. | NH3•H2O的电离常数K=10-4 |
19.下列大小顺序排列不正确的组合是( )
| A. | 气态氢化物的稳定性:H2O>H2S>SiH4 | |
| B. | 离子半径:Cl->O2->Mg2+ | |
| C. | 物质酸性:H3PO4>H2SO4>HClO4 | |
| D. | 熔点:KCl>K |
16.下表中的数据是破坏1mol物质中的化学键所消耗的能量(KJ)
在一定条件下,1molH2与1molCl2反应生成2molHCl的能量变化为( )
| 物质 | Cl2 | Br2 | I2 | HCl | HBr | HI | H2 |
| 能量(kJ) | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
| A. | 放出248 kJ 热量 | B. | 吸收248 kJ 热量 | C. | 放出183kJ 热量 | D. | 吸收183 kJ 热量 |
13.下列化学用语正确的是( )
| A. | 氯化氢的电子式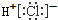 | B. | 镁的原子结构示意图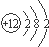 | ||
| C. | 乙酸的结构简式C2H4O2 | D. | HClO的结构式H-Cl-O |
17.将FeO与Cu(NO3)2的混合物9.08g全部溶于300mL、1mol/L的盐酸中,有部分Fe2+被酸性条件下的NO3-氧化(其化学反应方程式为:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O),放出NO气体448mL(标准状况);继续向溶液中通入一定量的Cl2恰好将溶液中的Fe2+完全氧化;再加入10g过量的铁粉,充分反应放出H2,过滤,得到不溶固体.下列叙述不正确的是( )
| A. | Cu(NO3)2的物质的量为0.01mol | B. | 通入Cl2的体积(标准状况)为448mL | ||
| C. | 放出H2的体积(标准状况)为112mL | D. | 得到不溶固体的质量为6.72g |
18.在碘水中加入适量的CCl4振荡后,观察到的现象为( )
| A. | 上层液体呈紫红色 | B. | 下层液体呈褐色 | ||
| C. | 上层液体呈深褐色 | D. | 下层液体呈紫红色 |
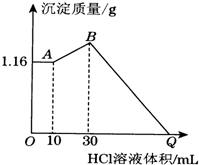 把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16g白色沉淀,在所得的浊液中逐滴加入1mol•L-1 HCl溶液,加入HCl溶液的体积与生成沉淀的质量关系如图所示,试回答:
把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16g白色沉淀,在所得的浊液中逐滴加入1mol•L-1 HCl溶液,加入HCl溶液的体积与生成沉淀的质量关系如图所示,试回答: