题目内容
18.室温时10mL某气态烃与过量氧气混合,完全燃烧后的产物通过浓硫酸,再恢复到室温,气体体积减少了30mL,剩余气体再通过苛性钠溶液,体积又减少了30mL.求气态烃的分子式及结构简式.分析 室温下气态烃与过量的氧气反应的化学方程式:CxHy+(x+$\frac{y}{4}$)O2$\stackrel{点燃}{→}$xCO2+$\frac{y}{2}$H2O(l),利用差量法计算出有机物分子中的H原子数;再把这些气体通过NaOH溶液气体体积,又减少了30mL,减少的气体为二氧化碳气体体积,据此可计算出该烃中含有C原子数,从而确定该烃的分子式.
解答 解:设烃为CxHy,
CxHy+(x+$\frac{y}{4}$)O2$\stackrel{点燃}{→}$xCO2+$\frac{y}{2}$H2O(l),△V
1 x+$\frac{y}{4}$ x 1+$\frac{y}{4}$
10 30
$\frac{1}{10}=\frac{1+\frac{y}{4}}{30}$,解得y=8,
剩余气体再通过苛性钠溶液,体积又减少了30mL,减少的气体为二氧化碳,
相同条件下气体的体积之比等于物质的量之比,则该烃中含有C原子数为$\frac{30mL}{10mL}$=3,
所以该有机物分子式为C3H8,结构简式为CH3CH2CH3,
答:气态烃的分子式为 C3H8 ,结构简式为CH3CH2CH3.
点评 本题考查有机物的推断,为高频考点,把握有机物燃烧规律、体积差计算为解答的关键,侧重分析、计算及推断能力的考查,题目难度不大.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案
相关题目
8.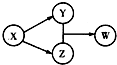 X、Y、Z、W四种物质的转化关系如图所示(部分反应物与产物已略),下列组合中不符合该关系的是( )
X、Y、Z、W四种物质的转化关系如图所示(部分反应物与产物已略),下列组合中不符合该关系的是( )
 X、Y、Z、W四种物质的转化关系如图所示(部分反应物与产物已略),下列组合中不符合该关系的是( )
X、Y、Z、W四种物质的转化关系如图所示(部分反应物与产物已略),下列组合中不符合该关系的是( )| A | B | C | D | |
| X | HCl | Na2O2 | Na2CO3 | Al |
| Y | FeCl2 | NaOH | CO2 | Na[Al(OH)4] |
| Z | Cl2 | Na2CO3 | CaCO3 | AlCl3 |
| W | FeCl3 | NaHCO3 | Ca(HCO3)2 | Al(OH)3 |
| A. | A | B. | B | C. | C | D. | D |
6.下列描述正确的是( )
| A. | 伴随有能量变化的物质变化都是化学变化 | |
| B. | 同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H不同 | |
| C. | 已知相同条件下2SO2(g)+O2(g)?2SO3(g)△H1,反应2SO2(s)+O2(g)?2SO3(g)△H2,则△H1>△H2 | |
| D. | 在稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ/mol,若将含0.5 mol H2SO4的浓H2SO4与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ |
10.已知:A(g)+2B(g)═C(g)+D(g)△H=a kJ•mol-1(a<0),下列说法正确的是( )
| A. | A(g)的能量一定高于C(g)的能量 | |
| B. | 该反应不需要加热 | |
| C. | 1 mol A(g)和2 mol B(g)的总能量高于1 mol C(g)的能量 | |
| D. | 该反应表示:1 mol A(g)和2 mol B(g)在一定条件下反应放出的热量为a kJ |
8.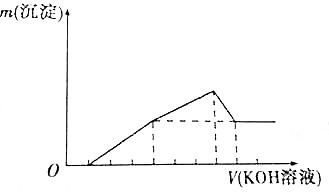 把镁铝合金用稀H2SO4溶解,加入KOH溶液的体积与生成沉淀的质量关系如图所示,则合金中镁与铝的质量之比为( )
把镁铝合金用稀H2SO4溶解,加入KOH溶液的体积与生成沉淀的质量关系如图所示,则合金中镁与铝的质量之比为( )
 把镁铝合金用稀H2SO4溶解,加入KOH溶液的体积与生成沉淀的质量关系如图所示,则合金中镁与铝的质量之比为( )
把镁铝合金用稀H2SO4溶解,加入KOH溶液的体积与生成沉淀的质量关系如图所示,则合金中镁与铝的质量之比为( )| A. | 1:1 | B. | 8:9 | C. | 2:3 | D. | 4:3 |
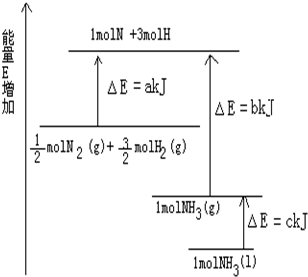 已知化学反应N2+3H2═2NH3的能量变化如图所示,
已知化学反应N2+3H2═2NH3的能量变化如图所示,