题目内容
9.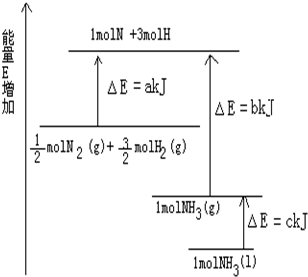 已知化学反应N2+3H2═2NH3的能量变化如图所示,
已知化学反应N2+3H2═2NH3的能量变化如图所示,(1)1mol N 和3mol H 生成1mol NH3(g)是释放能量的过程(填“吸收”或“释放”).
(2)$\frac{1}{2}$N2(g)+$\frac{3}{2}$H2(g)═NH3(g);△H=(a-b)kJ/mol
、
(3)N2(g)和H2生成NH3(l)的热化学方程式为
N2(g)+3H2(g)=2NH3(1)△H=2(a-b-c)kJ•mol-1.
分析 根据反应热等于反应物总能量减去生成物总能量计算反应热并书写热化学方程式,注意反应物的物质的量和生成物的聚集状态,由图可以看出,$\frac{1}{2}$molN2(g)+$\frac{3}{2}$molH2(g)的能量为akJ,1molNH3(g)的能量为bkJ,所以$\frac{1}{2}$N2(g)+$\frac{3}{2}$H2(g)=NH3(g);△H=(a-b)kJ/mol,
而1mol的NH3(g)转化为1mol的NH3(l)放出的热量为ckJ,所以有:$\frac{1}{2}$N2(g)+$\frac{3}{2}$H2(g)=NH3(l);△H=(a-b-c)kJ/mol,
即:N2(g)+3H2(g)=2NH3(1);△H=2(a-b-c)kJ•mol-1.
解答 解:(1)由图可以看出,1molN和3molH的总能量大于1mol NH3(g)的能量,则生成NH3(g)的过程为释放能量的过程,
故答案为:释放;
(2)由图可以看出,$\frac{1}{2}$molN2(g)+$\frac{3}{2}$molH2(g)的能量为akJ,1molNH3(g)的能量为bkJ,所以$\frac{1}{2}$N2(g)+$\frac{3}{2}$H2(g)=NH3(g)△H=(a-b)kJ/mol,
故答案为:(a-b)kJ/mol;
(3)由(2)可知$\frac{1}{2}$N2(g)+$\frac{3}{2}$H2(g)=NH3(g)△H=(a-b)kJ/mol,而1mol的NH3(g)转化为1mol的NH3(l)放出的热量为ckJ,
所以有:$\frac{1}{2}$N2(g)+$\frac{3}{2}$H2(g)=NH3(l);△H=(a-b-c)kJ/mol,即:N2(g)+3H2(g)=2NH3(1);△H=2(a-b-c)kJ•mol-1.
故答案为:N2(g)+3H2(g)=2NH3(1)△H=2(a-b-c)kJ•mol-1.
点评 本题考查热化学方程式的书写,题目难度不大,注意书写热化学方程式的注意事项以及反应热的计算方法,注意根据1mol的NH3(g)转化为1mol的NH3(l)放出的热量为ckJ计算N2(g)和H2生成NH3(l)的热化学方程式中的△H为易错点.

| A. | 羟基的电子式: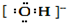 | B. | CH4分子的球棍模型: | ||
| C. | 乙烯的最简式:CH2 | D. | 氟离子的结构示意图: |
| A. | 氨气分子的电子式: | B. | 硫原子结构示意图: | ||
| C. | KCl的电子式: | D. | H2O2的电子式: |
| 化学键 | H-H | H-Cl | H-Br | CI-CI | Br-Br |
| 键能( KJ•mol-1) | 436 | 431 | 299 | 247 | 193 |
| A. | HCl | B. | HBr | C. | H2 | D. | Br2 |
| A. | 某主族元素的最高价含氧酸为HnROm,则其气态氢化物一般是H2m-nR | |
| B. | 除第ⅡA族族外,其余各族都有非金属元素 | |
| C. | 同一主族相邻的两种元素的原子序数之差可能为16 | |
| D. | 同一短周期元素的原子半径从左到右逐渐减小 |
| A. |  | B. |  | C. |  | D. |  |
 .
.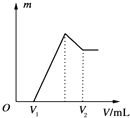 将0.1mol的镁、铝混合物溶于100mL、2mol•L-1的H2SO4溶液中,然后再滴加1mol•L-1的NaOH溶液.请回答:
将0.1mol的镁、铝混合物溶于100mL、2mol•L-1的H2SO4溶液中,然后再滴加1mol•L-1的NaOH溶液.请回答: