题目内容
6.下列描述正确的是( )| A. | 伴随有能量变化的物质变化都是化学变化 | |
| B. | 同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H不同 | |
| C. | 已知相同条件下2SO2(g)+O2(g)?2SO3(g)△H1,反应2SO2(s)+O2(g)?2SO3(g)△H2,则△H1>△H2 | |
| D. | 在稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ/mol,若将含0.5 mol H2SO4的浓H2SO4与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ |
分析 A.浓硫酸稀释、铵盐溶解等均有能量变化,但均为物理变化;
B.反应中△H与反应条件无关;
C.气态转化为固态,放出热量;
D.含0.5 mol H2SO4的浓H2SO4与含1 mol NaOH的溶液混合,生成1molH2O放出57.3kJ的热量,且浓硫酸稀释放热.
解答 解:A.浓硫酸稀释、铵盐溶解等均有能量变化,但均为物理变化,则伴随有能量变化的物质变化不一定是化学变化,故A错误;
B.反应中△H与反应条件无关,则同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H相同,故B错误;
C.气态转化为固态,放出热量,且△H1、△H2均为负值,可知相同条件下2SO2(g)+O2(g)?2SO3(g)△H1,反应2SO2(s)+O2(g)?2SO3(g)△H2,则△H1<△H2,故C错误;
D.含0.5 mol H2SO4的浓H2SO4与含1 mol NaOH的溶液混合,生成1molH2O放出57.3kJ的热量,且浓硫酸稀释放热,则该过程放出的热量大于57.3 kJ,故D正确;
故选D.
点评 本题考查反应热与焓变,为高频考点,把握反应中能量变化、焓变的判断为解答的关键,侧重分析与应用能力的考查,注意浓硫酸稀释为放热的物理变化,题目难度不大.

练习册系列答案
 孟建平名校考卷系列答案
孟建平名校考卷系列答案
相关题目
17.下列表示物质结构的化学用语或模型正确的是( )
| A. | 羟基的电子式: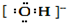 | B. | CH4分子的球棍模型: | ||
| C. | 乙烯的最简式:CH2 | D. | 氟离子的结构示意图: |
14.根据如表所列键能数据,下列分子中最不稳定的分子是( )
| 化学键 | H-H | H-Cl | H-Br | CI-CI | Br-Br |
| 键能( KJ•mol-1) | 436 | 431 | 299 | 247 | 193 |
| A. | HCl | B. | HBr | C. | H2 | D. | Br2 |
1.下列叙述正确的是( )
| A. | 某主族元素的最高价含氧酸为HnROm,则其气态氢化物一般是H2m-nR | |
| B. | 除第ⅡA族族外,其余各族都有非金属元素 | |
| C. | 同一主族相邻的两种元素的原子序数之差可能为16 | |
| D. | 同一短周期元素的原子半径从左到右逐渐减小 |
11.通常人们把拆开1mol某化学键所消耗的能量看成该化学键的键能,键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(△H),化学反应的(△H)等于反应物的总键能与生成物的总键能之差.
工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g) $\frac{\underline{\;高温\;}}{\;}$Si(s)+4HCl(g),该反应的反应热AH为( )
| 化学键 | Si-O | Si-Cl | H-H | H-Cl | Si-Si | Si-C |
| l键能/kJ•mol | 460 | 360 | 436 | 431 | 176 | 347 |
| A. | +412 kJ•mol-1 | B. | -412 kJ•mol-1 | C. | +236 kJ•mol-1 | D. | -236 kJ•mol-1 |
16.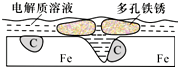 炒过菜的铁锅未及时洗净(残液中含NaCl),不久便会因被腐蚀而出现红褐色锈斑.腐蚀原理如右图所示,下列说法正确的是( )
炒过菜的铁锅未及时洗净(残液中含NaCl),不久便会因被腐蚀而出现红褐色锈斑.腐蚀原理如右图所示,下列说法正确的是( )
 炒过菜的铁锅未及时洗净(残液中含NaCl),不久便会因被腐蚀而出现红褐色锈斑.腐蚀原理如右图所示,下列说法正确的是( )
炒过菜的铁锅未及时洗净(残液中含NaCl),不久便会因被腐蚀而出现红褐色锈斑.腐蚀原理如右图所示,下列说法正确的是( )| A. | 腐蚀过程中,负极是C | |
| B. | Fe失去电子经电解质溶液转移给C | |
| C. | 正极的电极反应式为4OH--4e-═2H2O+O2↑ | |
| D. | 每生成1 mol铁锈(Fe2O3•xH2O)理论上消耗标准状况下的O233.6 L |
 .
. .
.