题目内容
1.由短周期元素构成的下列四种物质,转化关系如图.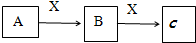
(1)若B与C相对分子质量相差16,C 能与水反应生成强酸,且A为固体单质,则A为A
(2)若C为发酵粉的主要成分之一,则X为CO2写出B→C离子反应方程式CO2+H2O+CO32-=2HCO3-.
分析 (1)若B与C相对分子质量相差16,氧原子的相对原子质量为16,说明BC都是氧化物,C 能与水反应生成强酸,证明C为酸性氧化物,且A为固体单质应为非金属单质判断为S,B为二氧化硫,C 为三氧化硫.溶于水发生反应SO3+H2O=H2SO4,
(2)C为发酵粉的主要成分之一,则C为碳酸氢钠,X为二氧化碳.A为氢氧化钠溶液,B为碳酸钠溶液.
解答 解:(1)若B与C相对分子质量相差16,氧原子的相对原子质量为16,说明BC都是氧化物,C 能与水反应生成强酸,证明C为酸性氧化物,且A为固体单质应为非金属单质判断A为S,B为二氧化硫,C 为三氧化硫.溶于水发生反应SO3+H2O=H2SO4,故答案为:S;
(2)C为发酵粉的主要成分之一,则C为碳酸氢钠,X为二氧化碳.A为氢氧化钠溶液,B为碳酸钠溶液;,CO2+2NaOH=Na2CO3+H2O,CO2+Na2CO3+H2O=2NaHCO3,B-C反应的离子方程式为:CO2+H2O+CO32-=2HCO3-,故答案为:CO2;CO2+H2O+CO32-=2HCO3-;
点评 本题考查了无机物的转化关系推断,主要是物质性质、反应特征、反应现象和物质组成特点的理解应用,掌握基础是解题关键,题目难度不大.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目
18.生产、生活中处处有化学,下列有关说法正确的是( )
| A. | 工业生产玻璃、水泥、漂白粉,均需要用石灰石为原料 | |
| B. | 某雨水样品放置一段时间后,PH由4.68变为4.00,是因为水中溶解的CO2增多 | |
| C. | 在结冰的路面上撒盐,是利用盐与水发生化学反应放出大量热量,促使冰雪融化 | |
| D. | 人类对于能源的利用大致可以分为三个时代:柴草能源、化石能源、多能源时代,目前,全球已主要处于多能源时代 |
16.下列各组溶液,只用试管和胶头滴管就可以鉴别的是( )
①AlCl3溶液和NaOH溶液
②Ca(HCO3)2溶液和NaOH溶液
③NaAlO2溶液和盐酸
④Al2(SO4)3溶液和氨水
⑤AgNO3溶液和氨水.
①AlCl3溶液和NaOH溶液
②Ca(HCO3)2溶液和NaOH溶液
③NaAlO2溶液和盐酸
④Al2(SO4)3溶液和氨水
⑤AgNO3溶液和氨水.
| A. | ①③⑤ | B. | ①②③ | C. | ②③④ | D. | ③④⑤ |
3.下列表示正确的是( )
| A. | 0.5mol氢 | B. | 1mol氧气 | C. | 1mole- | D. | 1mol氯化钠 |
6.已知弱酸的电离平衡常数如下表:下列选项正确的是( )
| 弱酸 | H2CO3 | 水杨酸(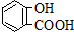 ) ) |
| 电离平衡常数(25℃) | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka1=1.3×10-3 Ka2=1.1×10-11 |
| A. | 常温下,等浓度、等体积的NaHCO3溶液pH小于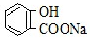 溶液pH 溶液pH | |
| B. | 常温下,等浓度、等体积的Na2CO3溶液和  溶液中所含离子总数前者小于后者 溶液中所含离子总数前者小于后者 | |
| C. |  +2NaHCO3→ +2NaHCO3→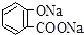 +2H2O+2CO2↑ +2H2O+2CO2↑ | |
| D. |  最多可与2molCO2反应 最多可与2molCO2反应 |
13.“春种一粒粟,秋收万颗子.”精选种子有利于提高农作物的产量,深圳市某农场工作人员配制了200kg某浓度的NaCl溶液选种,某学习小组取出731.25g NaCl溶液放置在一个大烧杯中,往烧杯中逐次加入AgNO3溶液测定其浓度,所得数据如图表所示.
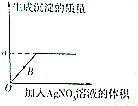 (1)生成沉淀的质量a=287.0g.
(1)生成沉淀的质量a=287.0g.
(2)在B点处,烧杯中溶液的溶质是NaNO3、NaCl(写化学式).
(3)该NaCl溶液的浓度是多少?(请写出详细的计算过程)
| 序号 | 1 | 2 | 3 | 4 | 5 |
| 每次加入AgNO溶液的体积/mL | 100 | 100 | 100 | 100 | 100 |
| 生成沉淀的质量/g | 71.75 | 143.5 | 215.25 | 287.0 | 287.0 |
 (1)生成沉淀的质量a=287.0g.
(1)生成沉淀的质量a=287.0g.(2)在B点处,烧杯中溶液的溶质是NaNO3、NaCl(写化学式).
(3)该NaCl溶液的浓度是多少?(请写出详细的计算过程)
10.关于有机物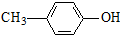 的叙述错误的是( )
的叙述错误的是( )
 的叙述错误的是( )
的叙述错误的是( )| A. | 分子式为C7H10O | B. | 含有羟基 | C. | 能发生加成反应 | D. | 含有苯环结构 |