题目内容
10.分子式为 C10H14且属于苯的同系物的同分异构体有______种( )| A. | 20种 | B. | 21 种 | C. | 22 种 | D. | 23 种 |
分析 C10H14的苯的同系物,侧链为烷基,
①苯环上只含1个侧链,则侧链为-C4H9,且连接苯环的C原子上含有H原子,所以只判断丁烷烷基的同分异构体即可;
②4个碳原子形成2个取代基,一个碳原子一定是甲基,两个碳原子一定是乙基,三个碳原子可能是-CH2CH2CH3 或-CH(CH3)2,两个取代基连在苯环上可能有邻、间、对三种情况;
③4个碳原子形成3个取代基,3个取代基为甲基、甲基、乙基,采取定两个甲基的位置,移动乙基,据此书写异构体判断;
④4个碳原子形成4个取代基,则取代基只能为甲基.
解答 解:C10H14的苯的同系物,侧链为烷基,
①苯环上只含1个侧链,则侧链为-C4H9,且连接苯环的C原子上含有H原子,丁烷烷基的碳链同分异构体有: ,共4种结构;
,共4种结构;
②4个碳原子形成2个取代基,一个碳原子一定是甲基,两个碳原子一定是乙基,三个碳原子可能是-CH2CH2CH3 或-CH(CH3)2,第一类两个取代基分别为
甲基和-CH2CH2CH3 或-CH(CH3)2,它们连接在苯环上又有邻、间、对三种情况,共有6种结构,第二类两个取代基均为乙基,它们连接在苯环上又有邻、间、对三种情况,共有3种结构,则总共9种结构;
③4个碳原子形成3个取代基,3个取代基为甲基、甲基、乙基,采取定两个甲基的位置,移动乙基,
若两个甲基为邻位位置,即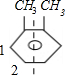 ,为对称结构,乙基有如图所示的2种取代位置,有2种结构;
,为对称结构,乙基有如图所示的2种取代位置,有2种结构;
若两个甲基为间位位置,即 ,为对称结构,乙基有如图所示的3种取代位置,有3种结构;
,为对称结构,乙基有如图所示的3种取代位置,有3种结构;
若两个甲基为对位位置,即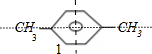 ,为对称结构,乙基有如图所示的1种取代位置,有1种结构;
,为对称结构,乙基有如图所示的1种取代位置,有1种结构;
共有6种结构;
④4个碳原子形成4个取代基,则取代基只能为甲基,共与3种结构,1,2,3,4-四甲基苯、1,2,3,5-四甲基苯和1,2,3,6-四甲基苯,共有3种结构;
所以属于苯的同系物的所有同分异构体共有:4+9+6+3=22种,
故选C.
点评 本题考查了同分异构体的书写方法,题目难度中等,明确同分异构体的书写原则为解答关键,注意掌握同分异构体的概念及书写方法,试题培养了学生的分析、理解能力及逻辑推理能力.

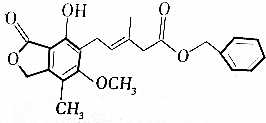
| A. | 该物质的化学式是C23H24O6 | |
| B. | 1mol该化合物最多可以与9molH2加成 | |
| C. | 酸性KMnO4溶液、溴水能与该物质发生氧化还原反应而褪色 | |
| D. | 该物质与FeCl3溶液作用可显红色,该反应可用于检验其中的酚羟基 |
| A. | CH3COOH的浓度比NaOH溶液大,反应后醋酸过量呈酸性 | |
| B. | CH3COOH溶液中水的电离程度大于NaOH溶液中水的电离程度 | |
| C. | 反应后溶液中的离子浓度一定是c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | |
| D. | 反应后的溶液中c(Na+)与c(CH3COO-)可能相等 |
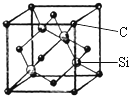 铜、镓、硒、硅等元素的化合物是生产第三代太阳能电池的重要材料.请回答:
铜、镓、硒、硅等元素的化合物是生产第三代太阳能电池的重要材料.请回答: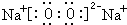 .X和Y组成的化合物中,既含有极性共价键又含有非极性共价键的是(用化学式表示)H2O2.
.X和Y组成的化合物中,既含有极性共价键又含有非极性共价键的是(用化学式表示)H2O2.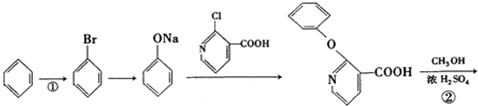

 +H2N-NH2→
+H2N-NH2→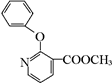 +CH3OH,
+CH3OH, ,
,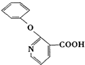 的分子式为C12H9O3N,它有多种同分异构体,其中符合下列条件的同分异构体共有4种.
的分子式为C12H9O3N,它有多种同分异构体,其中符合下列条件的同分异构体共有4种.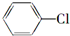 制备
制备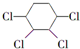
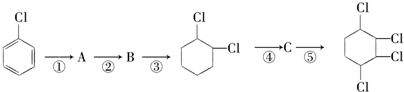
 B:
B: .
. +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$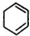 +2NaCl+2H2O
+2NaCl+2H2O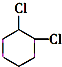 的含有六元碳环的同分异构体:
的含有六元碳环的同分异构体: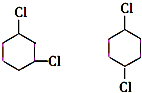
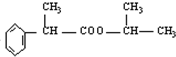
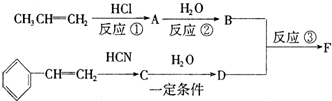
 .
. .
. .
.