题目内容
下列物质属于非电解质的是( )
| A、HNO3 |
| B、Cl2 |
| C、NH4NO3 |
| D、SO2 |
考点:电解质与非电解质
专题:
分析:非电解质是指:在水溶液和熔化状态下都不能导电的化合物,或导电不是自身电离出自由移动的离子造成.非电解质判断:必须是化合物,且溶液不导电,或导电不是自身电离出自由移动的离子造成,据此即可解答;
解答:
解:A.HNO3为化合物,其水溶液能导电,HNO3属于电解质,故A错误;
B.氯气是单质,不是化合物,不是非电解质,故B错误;
C.NH4NO3为化合物,其水溶液能导电,它属于电解质,故C错误;
D.二氧化硫为化合物,其水溶液能导电,为SO2与水反应,生成的亚硫酸电离出自由移动的离子导电,其本身不发生电离,所以SO2属于非电解质,故D正确;
故选D.
B.氯气是单质,不是化合物,不是非电解质,故B错误;
C.NH4NO3为化合物,其水溶液能导电,它属于电解质,故C错误;
D.二氧化硫为化合物,其水溶液能导电,为SO2与水反应,生成的亚硫酸电离出自由移动的离子导电,其本身不发生电离,所以SO2属于非电解质,故D正确;
故选D.
点评:本题考查非电解质,明确非电解质概念的要点是:化合物,且溶液不导电,或导电不是自身电离出自由移动的离子造成,注意大多数有机化合物都是非电解质,如,甘油、乙醇等,题目难度不大.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
某有机物A 7.4g与足量CuO共热后,所得气体产物依次通过盛有浓H2SO4和碱石灰的仪器,两仪器分别增重9g、17.6g;同温同压,A蒸汽的密度是H2的37倍,则能够与钠反应放出H2的A的同分异构体的数目为(不考虑立体异构)( )
| A、8 | B、6 | C、4 | D、2 |
下列说法正确的是( )
| A、1 molH2的质量是1 g |
| B、1 mol HCl的质量是36.5 g?mol-1 |
| C、Cl2的摩尔质量等于它的相对分子质量 |
| D、硫酸根离子的摩尔质量是96 g?mol-1 |
水的电离平衡曲线如图所示,下列说法不正确的是( )
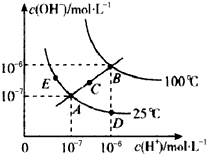

| A、从图中可以看出,水的电离是吸热过程 |
| B、若从A点到D点,可采用:温度不变在水中加入适量的NH4Cl固体 |
| C、在处于C点状态的溶液中:Na+、Al3+、CO32-、Cl-能够大量共存 |
| D、在处于E点状态的CH3COONa溶液中:c(Na+)>c(CH3COO-)>c(OH+)>c(H+) |
 表示碳原子,用
表示碳原子,用 表示氧原子,用
表示氧原子,用 表示氮原子,如图为气体转换的微观过程.请你根据图示回答下列问题:
表示氮原子,如图为气体转换的微观过程.请你根据图示回答下列问题: