题目内容
1.下列说法正确的是( )| A. | 能使pH试纸呈红色的溶液中可能大量存在以下离子:Na+、NH4+、I-、NO3- | |
| B. | 将CH3COOH溶液和NaOH溶液等体积混合,该溶液中一定存在的关系式为:c(Na+)=c(CH3COO-)+c(CH3COOH) | |
| C. | pH=3的NaHA溶液中粒子浓度大小为:c(Na+)>c(HA-)>c(A2-)>c(H2A)>c(OH-) | |
| D. | CuSO4溶液遇到闪锌矿(ZnS)慢慢转化为铜蓝(CuS),是因为ZnS的溶解度大于CuS |
分析 A.能使pH试纸呈红色的溶液呈酸性,离子之间发生氧化还原反应;
B.只有CH3 COOH和NaOH的物质的量相等时,混合后c( Na+)=c(CH3 COO-)+c(CH3COOH);
C.pH=3的NaHA溶液,说明电离HA-大于水解程度;
D.从难溶电解质的溶解平衡的角度分析.
解答 解:A.能使pH试纸呈红色的溶液呈酸性,I-、NO3-之间发生氧化还原反应,不能大量共存,故A错误;
B.只有CH3COOH和NaOH的物质的量相等时,混合后c(Na+)=c(CH3COO-)+c(CH3COOH),如二者的物质的量不能,则关系式不成立,故B错误;
C.pH=3的NaHA溶液,说明电离HA-大于水解程度,溶液中基本不存在H2A,c(OH-)>c(H2A),故C错误;
D.难溶电解质的溶解平衡及沉淀转化是溶解度大的物质向溶解度小的物质转化,ZnS能转化为CuS,所以CuS的溶解度小于ZnS的溶解度,故D正确.
故选D.
点评 本题考查较为综合,涉及离子浓度大小比较、离子共存、难溶电解质的溶解平衡等问题,为高频考点,侧重于学生的分析能力,难度不大.

练习册系列答案
相关题目
11. 日本一家公司日前宣布,他们已经开发并计划大量生产一种颠覆性的阳极和阴极都是碳材料的双碳性电池(放电原理示意如图所示),充电速度比普通的锂离子电池快20倍.放电时,正极反应Cn(PF6)+e-═PF6-+nC,负极反应LiCn-e-═Li++nC下列有关说法中正确的是( )
日本一家公司日前宣布,他们已经开发并计划大量生产一种颠覆性的阳极和阴极都是碳材料的双碳性电池(放电原理示意如图所示),充电速度比普通的锂离子电池快20倍.放电时,正极反应Cn(PF6)+e-═PF6-+nC,负极反应LiCn-e-═Li++nC下列有关说法中正确的是( )
 日本一家公司日前宣布,他们已经开发并计划大量生产一种颠覆性的阳极和阴极都是碳材料的双碳性电池(放电原理示意如图所示),充电速度比普通的锂离子电池快20倍.放电时,正极反应Cn(PF6)+e-═PF6-+nC,负极反应LiCn-e-═Li++nC下列有关说法中正确的是( )
日本一家公司日前宣布,他们已经开发并计划大量生产一种颠覆性的阳极和阴极都是碳材料的双碳性电池(放电原理示意如图所示),充电速度比普通的锂离子电池快20倍.放电时,正极反应Cn(PF6)+e-═PF6-+nC,负极反应LiCn-e-═Li++nC下列有关说法中正确的是( )| A. | a极为电池的负极 | |
| B. | A-为OH- | |
| C. | 电池充电时阴极反应为:LiCn+e-═Li++nC | |
| D. | 充电时,溶液中A-从b极向a极迁移 |
12.化学反应中,有时存在一种物质过量,另一种物质仍不能完全反应的特殊情况,下列反应中属于这种情况的是( )
①过量的锌与18mol/L硫酸溶液反应
②过量的氢气与少量的氮气在催化剂存在和一定条件下充分反应
③加热条件下浓盐酸与过量MnO2 反应
④加热条件下过量铜与浓硫酸反应
⑤过量稀硫酸与块状石灰石反应.
①过量的锌与18mol/L硫酸溶液反应
②过量的氢气与少量的氮气在催化剂存在和一定条件下充分反应
③加热条件下浓盐酸与过量MnO2 反应
④加热条件下过量铜与浓硫酸反应
⑤过量稀硫酸与块状石灰石反应.
| A. | ②③④⑤ | B. | ②③④ | C. | ①③④ | D. | ①②③④⑤ |
9.BLAl2(SO4)3溶液中含有agAl3+,则SO42-的物质的量浓度为( )
| A. | $\frac{3a}{2B}$mol/L | B. | $\frac{a}{27B}$mol/L | C. | $\frac{a}{18B}$mol/L | D. | $\frac{2a}{81B}$mol/L |
13.在一密闭容器中,用一不漏气的滑动活塞隔开,常温时在左边充入$\frac{3}{4}$体积H2和O2混合气体,在右边充入$\frac{1}{4}$体积N2,若将左边混合气体点燃充分反应后恢复到原温,活塞停留在中间,则反应前混合气体中H2和O2的体积比可能是( )
| A. | 7:2 | B. | 4:5 | C. | 5:4 | D. | 2:7 |
13.下列说法正确的是( )
| A. | 所有的化学反应都有能量变化 | |
| B. | 只要有能量的变化,一定发生了化学反应 | |
| C. | 据能量守恒定律,反应物的总能量一定等于生成物的总能量 | |
| D. | 需要加热才能发生的反应一定是吸热反应 |
 .
. .
.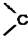 =O$→_{H+}^{ROH}$
=O$→_{H+}^{ROH}$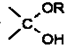 $→_{H+}^{ROH}$
$→_{H+}^{ROH}$ 写出由乙烯、甲醇为有机原料制备化合物
写出由乙烯、甲醇为有机原料制备化合物 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2$\stackrel{Br_{2}}{→}$CH2Br•CH2Br.
的合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2$\stackrel{Br_{2}}{→}$CH2Br•CH2Br.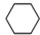 (g)$?_{高温}^{Pt-Sn/Al_{2}O_{3}}$
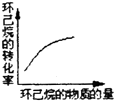
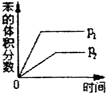
(g)$?_{高温}^{Pt-Sn/Al_{2}O_{3}}$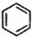 (g)+3H2(g)△H>0,若该反应在恒容的密闭容器中进行,下列有关该反应的图象判断正确的是( )
(g)+3H2(g)△H>0,若该反应在恒容的密闭容器中进行,下列有关该反应的图象判断正确的是( )