题目内容
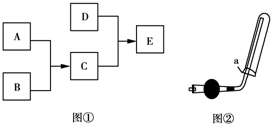 已知A、B、C、D为气体,其中A为黄绿色,D极易溶于水,形成的溶液可使酚酞变红,它们之间的转化关系如图①所示:
已知A、B、C、D为气体,其中A为黄绿色,D极易溶于水,形成的溶液可使酚酞变红,它们之间的转化关系如图①所示:(1)将气体B点燃,把导管伸入盛满气体A的集气瓶,反应过程中的实验现象有
①放热 ②黄绿色褪去 ③瓶口有白雾 ④瓶口有白烟
⑤安静燃烧,发出黄色火焰 ⑥安静燃烧,发出苍白色火焰
(2)实验室制D的化学方程式为
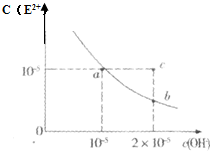
(3)实验室可用如图②所示装置收集D,下列叙述正确的是
①D气体不能用排水法收集
②干燥管里盛有碱石灰
③图②中的a为棉花团,其作用是防止氨气逸出
(4)气体D催化氧化的化学方程式为
(5)物质E的化学式是
①电解质;②化合物;③混合物;④纯净物;⑤非电解质;⑥盐.
考点:无机物的推断,氯气的化学性质,氨的化学性质
专题:推断题
分析:A为黄绿色气体,应为Cl2,D极易溶于水,形成的溶液可使酚酞变红,应为NH3,A、B、C、D为气体,则B是H2,C是HCl,所以E是NH4Cl,结合对应物质的性质以及题目要求可解答该题.
解答:
解:A为黄绿色气体,应为Cl2,D极易溶于水,形成的溶液可使酚酞变红,应为NH3,A、B、C、D为气体,则B是H2,C是HCl,所以E是NH4Cl,
(1)氢气在氯气中安静的燃烧,火焰苍白色,黄绿色逐渐褪去,瓶口有白雾(氯化氢气体与空气中的小水滴结合)出现,燃烧反应都是放热反应,所以选①②③⑥,
故答案为:①②③⑥;
(2)实验室制氨气的化学方程式为:Ca(OH)2+2NH4Cl
CaCl2+H2O+2NH3↑,
故答案为:Ca(OH)2+2NH4Cl
CaCl2+H2O+2NH3↑;
(3)氨气极易溶于水,不能用排水法收集,氨气溶于水显碱性,可用碱石灰干燥,图②中的a应为湿润红色石蕊试纸,检验氨气是否收集满,所以答案选①②,
故答案为:①②;
(4)氨气发生催化氧化的化学方程式为:4NH3+5O2
4NO+6H2O,
故答案为:4NH3+5O2
4NO+6H2O;
(5)E是氯化铵,化学式为NH4Cl,它是化合物,是纯净物,是盐,是电解质,所以答案选①②④⑥,
故答案为:NH4Cl;①②④⑥.
(1)氢气在氯气中安静的燃烧,火焰苍白色,黄绿色逐渐褪去,瓶口有白雾(氯化氢气体与空气中的小水滴结合)出现,燃烧反应都是放热反应,所以选①②③⑥,
故答案为:①②③⑥;
(2)实验室制氨气的化学方程式为:Ca(OH)2+2NH4Cl
| ||
故答案为:Ca(OH)2+2NH4Cl
| ||
(3)氨气极易溶于水,不能用排水法收集,氨气溶于水显碱性,可用碱石灰干燥,图②中的a应为湿润红色石蕊试纸,检验氨气是否收集满,所以答案选①②,
故答案为:①②;
(4)氨气发生催化氧化的化学方程式为:4NH3+5O2
| ||
| △ |
故答案为:4NH3+5O2
| ||
| △ |
(5)E是氯化铵,化学式为NH4Cl,它是化合物,是纯净物,是盐,是电解质,所以答案选①②④⑥,
故答案为:NH4Cl;①②④⑥.
点评:本题考查物质推断、氢气与氯气反应的现象、氨气的性质与制备、物质的分类等,比较基础,注意根据物质的颜色、状态、水溶性等性质作为该题的突破口,把握相关物质的实验室制备.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列关于SiO2的说法正确的是( )
| A、用来制造光导纤维 |
| B、能与盐酸发生反应 |
| C、能跟水反应生成硅酸 |
| D、用作半导体材料 |
 A、B、C、D、E、F、G为原子序数依次递增的7种短周期主族元素.A、B元素的最高正价与最低负价的代数和均为零;C元素是植物生长三大营养元素之一;D的单质具有强氧化性,其氢化物能和一种半导体材料反应生成常温常压下的两种气体;E原子核外K层电子数与M层电子数相等;F原子的价电子数等于电子层数的两倍.请回答下列问题:
A、B、C、D、E、F、G为原子序数依次递增的7种短周期主族元素.A、B元素的最高正价与最低负价的代数和均为零;C元素是植物生长三大营养元素之一;D的单质具有强氧化性,其氢化物能和一种半导体材料反应生成常温常压下的两种气体;E原子核外K层电子数与M层电子数相等;F原子的价电子数等于电子层数的两倍.请回答下列问题: NO、NO2、SO2、CO等均为大气污染物,研究这些气体的吸收和处理意义重大.请回答下列问题:
NO、NO2、SO2、CO等均为大气污染物,研究这些气体的吸收和处理意义重大.请回答下列问题: