题目内容
(1)根据构造原理写出29号元素的基态的电子排布式
(2)写出下列原子的电子排布图①N
(3)用VSEPR模型和杂化轨道理论相关知识填表
(4)白磷分子的空间构型为 ,每个P原子与 个P原子结合成共价键.若将1分子白磷中的所有P-P键打开并各插入一个氧原子,共可结合 个氧原子,若每个P原子上的孤对电子再与氧原子配位,就可以得到磷的另一种氧化物 (填分子式).
(2)写出下列原子的电子排布图①N
(3)用VSEPR模型和杂化轨道理论相关知识填表
| 微粒 | 孤电子对数 | 杂化轨道数 | 中心原子轨道杂化形式 | 微粒的空间构型 |
| SO2 | ||||
| NH4+ | ||||
| CO32- |
考点:原子核外电子排布,判断简单分子或离子的构型,原子轨道杂化方式及杂化类型判断
专题:化学键与晶体结构
分析:(1)根据元素符号,判断元素原子的核外电子数,再根据构造原理来写;
(2)N原子核外有7个电子,分别位于1S、2S、2P轨道;
(3)根据价电子对互斥理论确定微粒的空间构型和原子的杂化方式,价层电子对个数=σ键个数+孤电子对个数;
(4)根据白磷分子的空间构型判断含有的共价键数目;白磷含有6个共价键,可形成化合物P4O10.
(2)N原子核外有7个电子,分别位于1S、2S、2P轨道;
(3)根据价电子对互斥理论确定微粒的空间构型和原子的杂化方式,价层电子对个数=σ键个数+孤电子对个数;
(4)根据白磷分子的空间构型判断含有的共价键数目;白磷含有6个共价键,可形成化合物P4O10.
解答:
解:(1)29号元素为Cu元素,原子核外有29个电子,所以核外电子排布式为:1s22s22p63s23p63d104s1,故答案为:1s22s22p63s23p63d104s1;
(2)N原子核外有7个电子,分别位于1S、2S、2P轨道,其轨道表示式为 ,故答案为:
,故答案为: ;
;
(3)SO2中S原子的价层电子对个数=δ键数+孤对电子对数=2+
(6-2×2)=3,含孤电子对数为1,杂化轨道数3,采取sp2杂化,结构为V形
NH4+中N原子的价层电子对个数=δ键数+孤对电子对数=4+0=4,含孤电子对数为0,杂化轨道数4,采取sp3杂化,结构为正四面体形;
CO32-中C原子的价层电子对个数=σ键个数+孤电子对个数=3+
(4+2-3×2)=3,杂化轨道数3,采用原子杂化方式是sp2,为平面三角形结构;
故答案为:
;
(4)白磷为正四面体结构,每个P原子与3个P原子结合成共价键,每个分子中含有6个共价键,若将1分子白磷中的所有P-P键打开并各插入一个氧原子,共可结合6个O原子,若每个P原子上的孤对电子分别再以配位键连接一个氧原子,还可结合4个O原子,则可形成化合物P4O10,
故答案为:正四面体;3;6;P4O10.
(2)N原子核外有7个电子,分别位于1S、2S、2P轨道,其轨道表示式为
 ,故答案为:
,故答案为: ;
;(3)SO2中S原子的价层电子对个数=δ键数+孤对电子对数=2+
| 1 |
| 2 |
NH4+中N原子的价层电子对个数=δ键数+孤对电子对数=4+0=4,含孤电子对数为0,杂化轨道数4,采取sp3杂化,结构为正四面体形;
CO32-中C原子的价层电子对个数=σ键个数+孤电子对个数=3+
| 1 |
| 2 |
故答案为:
| 微粒 | 孤电子对数 | 杂化轨道数 | 中心原子轨道杂化形式 | 微粒的空间构型 |
| SO2 | 1 | 3 | sp2 | V形 |
| NH4+ | 0 | 4 | sp3 | 正四面体形 |
| CO32- | 0 | 3 | sp2 | 平面三角形 |
(4)白磷为正四面体结构,每个P原子与3个P原子结合成共价键,每个分子中含有6个共价键,若将1分子白磷中的所有P-P键打开并各插入一个氧原子,共可结合6个O原子,若每个P原子上的孤对电子分别再以配位键连接一个氧原子,还可结合4个O原子,则可形成化合物P4O10,
故答案为:正四面体;3;6;P4O10.
点评:本题考查较为综合,涉及电子排布式、电子排布图、杂化类型以及分子的立体构型的判断、白磷的结构等问题,题目难度中等,本题把握价层电子对互斥理论的应用.

练习册系列答案
相关题目
分离氯化钠和单质溴的水溶液,采取的正确方法是( )
| A、分液 | B、萃取 |
| C、蒸馏 | D、蒸馏、萃取、分液都可以 |
下列各组中两个溶液间的反应,均可用同一离子方程式表示的是( )
| A、HCl和Na2CO3 HCl和NaHCO3 |
| B、AgNO3和HCl AgNO3和H2SO4 |
| C、BaCl2和Na2SO4 Ba(OH)2和CuSO4 |
| D、KOH和CuCl2 Ba(OH)2和CuCl2 |
下列配制的溶液浓度偏高的是( )
| A、配制盐酸溶液用量筒量取盐酸时俯视刻度线 |
| B、浓H2SO4稀释后未经冷却即注入容量瓶配制 |
| C、配制100mL1mol/L Na2CO3溶液时,砝码放在托盘天平左盘 |
| D、配制盐酸溶液定容时,仰视容量瓶刻度线 |
 将1.0molCH4和2.0molH2O(g)通入容积为100L的反应室中,在一定条件下发生反应:CH4(g)+H2O(g)?CO(g)+3H2(g).测得在一定压强下的平衡转化率与温度的关系如图所示,下列说法错误的是( )
将1.0molCH4和2.0molH2O(g)通入容积为100L的反应室中,在一定条件下发生反应:CH4(g)+H2O(g)?CO(g)+3H2(g).测得在一定压强下的平衡转化率与温度的关系如图所示,下列说法错误的是( )| A、该反应为吸热反应 |
| B、100℃时,该反应的平衡常数K=7.2×10-5 mol2?L-2 |
| C、为提高甲烷的转化率,可增加甲烷与水的投料比 |
| D、若100℃时达到平衡所需时间为5min,那么0~5min内υ(H2)=0.0024mol?L-1?min-1 |
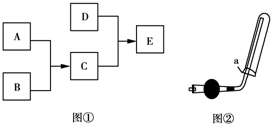 已知A、B、C、D为气体,其中A为黄绿色,D极易溶于水,形成的溶液可使酚酞变红,它们之间的转化关系如图①所示:
已知A、B、C、D为气体,其中A为黄绿色,D极易溶于水,形成的溶液可使酚酞变红,它们之间的转化关系如图①所示: 有A、B、C、D、E五种短周期元素,且相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示.E的氢氧化物是两性氢氧化物,且E的阳离子与A的阴离子核外电子层结构相同.请回答下列问题:
有A、B、C、D、E五种短周期元素,且相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示.E的氢氧化物是两性氢氧化物,且E的阳离子与A的阴离子核外电子层结构相同.请回答下列问题: 根据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图,其中盐桥内装琼脂饱和KNO3溶液.请回答下列问题:
根据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图,其中盐桥内装琼脂饱和KNO3溶液.请回答下列问题: