题目内容
某生提出,下列方法也可以炼制钢铁:FeO(s)+C(s)=Fe(s)+CO(g)△H>0,△S>0,对于上述反应,下列说法正确的是( )
| A、低温下自发进行,高温下非自发进行 |
| B、任何温度下均为自发进行 |
| C、任何温度下均为非自发进行 |
| D、高温下自发进行,低温下非自发进行 |
考点:焓变和熵变
专题:化学反应中的能量变化
分析:依据反应自发进行的判断依据分析,△H-T△S<0,反应自发进行;
解答:
解:FeO(s)+C(s)=Fe(s)+CO(g)△H>0,△S>0,
A、低温下可以存在,△H-T△S>0,自发不能进行,高温下可以存在,△H-T△S<0,可以自发进行,故A错误;
B、△H>0,△S>0,低温下反应非自发进行,故B错误;
C、△H>0,△S>0,高温下反应自发进行,故C错误;
D、高温下,△H-T△S<0,反应自发进行,低温下,△H-T△S>0,反应非自发进行,故D正确;
故选D.
A、低温下可以存在,△H-T△S>0,自发不能进行,高温下可以存在,△H-T△S<0,可以自发进行,故A错误;
B、△H>0,△S>0,低温下反应非自发进行,故B错误;
C、△H>0,△S>0,高温下反应自发进行,故C错误;
D、高温下,△H-T△S<0,反应自发进行,低温下,△H-T△S>0,反应非自发进行,故D正确;
故选D.
点评:本题考查了化学反应自发进行的判断依据和反应特征分析判断应用,掌握基础是关键,题目较简单.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
糖类、油脂、蛋白质为基本营养物质.下列有关说法正确的是( )
| A、蛋白质中只含C、H、O三种元素 |
| B、油脂在人体中发生水解的产物是氨基酸 |
| C、糖类的主要成分是高级脂肪酸甘油酯 |
| D、油脂、蛋白质都能发生水解反应 |
在一定条件下,Na2CO3溶液存在水解平衡:CO32-+H2O???HCO3-+OH-,下列说法正确的是( )
| A、稀释溶液,水解平衡常数增大 | ||||||
B、升高温度,
| ||||||
| C、通入CO2,平衡右移动 | ||||||
| D、加入NaOH(s),溶液pH减小 |
下列液体均处于25℃,有关叙述正确的是( )
| A、某物质的溶液pH<7,则该物质一定是酸或强酸弱碱盐 |
| B、Na2CO3溶液加水稀释后,恢复至原温度,pH和Kw均减小 |
| C、pH=5.6的CH3COOH与CH3COONa混合溶液中,c(Na+)>c(CH3COO-) |
| D、pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的100倍 |
下列说法正确的是( )
| A、水的电离方程式:H2O═H++OH- |
| B、升高温度,水的电离程度增大 |
| C、在NaOH溶液中没有H+,在HCl溶液中没有OH- |
| D、纯水中c(H+)=10-7 mol?L-1 |
下列说法正确的是( )
| A、有气体参加的化学反应,若增大压强,可增加活化分子的百分数,从而使反应速率增大 |
| B、催化剂不参与反应,但能降低活化能增大活化分子的百分数,从而增大反应速率 |
| C、增大反应物浓度,可增大活化分子的百分数,从而使单位时间有效碰撞次数增多 |
| D、升高温度能使化学反应速率增大,主要原因是增大了反应物分子中活化分子的百分数 |
下列有关四个常用电化学装置的叙述正确的是( )


| A、图Ⅰ所示电池中,MnO2作催化剂 |
| B、图Ⅱ所示电池放电过程中,硫酸浓度不断增大 |
| C、图Ⅲ所示装置工作过程中,电解质溶液中Cu2+浓度始终不变 |
| D、图Ⅳ所示电池中,Ag2O作氧化剂,在电池工作过程中被还原为Ag |
下列有关说法正确的是( )
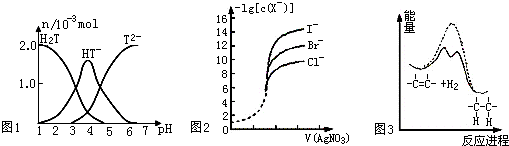

| A、常温下,向20mL0.1mol?L-1酒石酸(用H2T表示)溶液中逐滴滴加等物质的量浓度的NaOH溶液.有关微粒的物质的量与混合溶液的pH有如图1,则当VNaOH=10mL时,溶液中存在2C(Na+)=C(H2T)+C(HT-)+C(T2-) | ||
| B、用0.0100mol?L-1硝酸银标准溶液,滴定浓度均为0.100mol?L-1的 Cl-、Br-及I-的混合溶液,由图2曲线,可确定首先沉淀的是Cl- | ||
C、已知25℃、101kPa时:①2Na(s)+
| ||
| D、由图3可说明烯烃与H2加成反应是放热反应,虚线表示在有催化剂的条件下进行 |