题目内容
下列说法正确的是( )
| A、有气体参加的化学反应,若增大压强,可增加活化分子的百分数,从而使反应速率增大 |
| B、催化剂不参与反应,但能降低活化能增大活化分子的百分数,从而增大反应速率 |
| C、增大反应物浓度,可增大活化分子的百分数,从而使单位时间有效碰撞次数增多 |
| D、升高温度能使化学反应速率增大,主要原因是增大了反应物分子中活化分子的百分数 |
考点:活化能及其对化学反应速率的影响
专题:化学反应速率专题
分析:增大压强、浓度,单位体积活化分子的数目增多,升高温度、加入催化剂活化分子的百分数增大,反应速率加快由此分析解答.
解答:
解:A、有气体参加的化学反应,若增大压强,活化分子的百分数不变,单位体积活化分子总数增加,从而使反应速率,故A错误;
B、催化剂参与反应,但能降低活化能增大活化分子的百分数,从而增大反应速率增大,故B错误;
C、增大反应物浓度,单位体积活化分子的数目增多,从而使单位时间有效碰撞次数增多,故C错误;
D、升高温度提高活化分子百分数,使化学反应速率增大,故D正确;
故选D.
B、催化剂参与反应,但能降低活化能增大活化分子的百分数,从而增大反应速率增大,故B错误;
C、增大反应物浓度,单位体积活化分子的数目增多,从而使单位时间有效碰撞次数增多,故C错误;
D、升高温度提高活化分子百分数,使化学反应速率增大,故D正确;
故选D.
点评:本题考查影响活化分子的因素,题目难度不大,注意相关知识的积累,学习中注意温度、浓度、压强、催化剂对反应速率的影响的根本原因是影响活化分子的浓度或百分数.

练习册系列答案
相关题目
化学与科技、社会、环境密切相关.下列有关说法正确的是( )
| A、pH小于7的雨水被称为酸雨 |
| B、明矾溶于水可产生具有吸附性的胶体粒子,常用于饮用水的杀菌消毒 |
| C、推广使用燃煤脱硫技术,主要是为了防治SO2污染 |
| D、PM2.5是指大气中直径小于或等于2.5微米(2.5×10-6m)的细小可吸入颗粒物,其与空气形成的分散系属于胶体 |
化学反应4A(s)+3B(g)?2C(g)+D(g),经2min,B的浓度减少0.6mol/L.对此反应速率的表示正确的是( )
| A、用A表示的反应速率是0.4 mol?(L?min)-1 |
| B、分别用B、C、D表示的反应速率其比值是3:2:1 |
| C、2 min末的反应速率用B表示是0.3 mol?(L?min)-1 |
| D、2 min内,v正(B)和v逆(C)表示的反应速率的值都是逐渐减小的 |
某生提出,下列方法也可以炼制钢铁:FeO(s)+C(s)=Fe(s)+CO(g)△H>0,△S>0,对于上述反应,下列说法正确的是( )
| A、低温下自发进行,高温下非自发进行 |
| B、任何温度下均为自发进行 |
| C、任何温度下均为非自发进行 |
| D、高温下自发进行,低温下非自发进行 |
下列过程不需要通电就能进行的是( )
| A、电化学腐蚀 | B、电镀 |
| C、电解 | D、电泳 |
有关物质的性质可以用元素周期律解释的是( )
| A、酸性:HCl>H2S>H2O |
| B、密度:Na>K>Li |
| C、沸点:NH3>AsH3>PH3 |
| D、稳定性:HF>HCl>HBr |
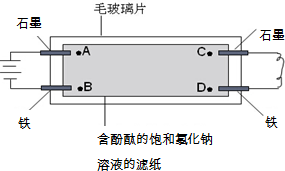 如图所示,在毛玻璃片上放有一张浸有含酚酞的饱和氯化钠溶液的滤纸,滤纸上点有A、B、C、D四个点(指靠近电极的溶液).有关说法正确的是 ( )
如图所示,在毛玻璃片上放有一张浸有含酚酞的饱和氯化钠溶液的滤纸,滤纸上点有A、B、C、D四个点(指靠近电极的溶液).有关说法正确的是 ( )| A、A点比B点先出现红色 |
| B、B点比A点先出现红色 |
| C、A点比C点先出现红色 |
| D、D点比C点先出现红色 |
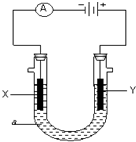 电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.
电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.