题目内容
4.乙稀利(C2H6ClO3P)植物生长调节剂,它可由环氧乙烧和PCl3为原料合成.相关表示不正确的是( )| A. | 环氧乙烷的结构简式:C2H4O | B. | 中子数为16的磷原子:${\;}_{15}^{16}$P | ||
| C. | 氯原子的结构示意图: | D. | PC13的电子式: |
分析 A.C2H4O为分子式,不是结构简式;
B.元素符号的质量数=质子数+中子数,元素符号的左上角为质量数、左下角为质子数;
C.氯原子的核电荷数=核外电子总数为17,最外层含有7个电子;
D.漏掉了P原子的1对未成键电子对.
解答 解:A.环氧乙烷的结构简式为: ,C2H4O为环氧乙烷的分子式,故A错误;
,C2H4O为环氧乙烷的分子式,故A错误;
B.中子数为16的磷原子的质量数=15+16=31,该原子正确的表示方法为:1531P,故B错误;
C.氯原子的核电荷数、核外电子总数都是17,其原子的结构示意图为: ,故C正确;
,故C正确;
D.PC13的电子式中,P、Cl原子最外层都满足8电子稳定结构,其正确的电子式为 ,故D错误;
,故D错误;
故选C.
点评 本题考查了常见化学用语的表示方法,题目难度不大,涉及电子式、结构简式、原子结构示意图、元素符号等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的规范答题能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.200mL Fe2(SO4)3溶液中含Fe3+5.6g,溶液中SO42-的物质的量浓度是( )
| A. | 0.5mol/L | B. | 0.75 mol/L | C. | 1 mol/L | D. | 0.25 mol/L |
12.在某200mL的混合溶液中,硝酸和硫酸的物质的量浓度分别为0.4mol/L、0.1mol/L,向溶液中加入3.84g铜粉,加热,待充分反应后,收集到标况下气体体积为( )
| A. | 1792mL | B. | 896mL | C. | 672mL | D. | 448mL |
19.某无色透明溶液中存在大量的H+、Cl-、NO3-,该溶液中还可能大量存在的是( )
| A. | HCO3- | B. | Cu2+ | C. | NH4+ | D. | Ag+ |
16.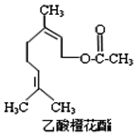 乙酸橙花酯是一种食用香料,其结构简式如图所示,关于该有机物的下列叙述中不正确的是( )
乙酸橙花酯是一种食用香料,其结构简式如图所示,关于该有机物的下列叙述中不正确的是( )
①分子式为C12H20O2
②能使酸性KMnO4溶液褪色,但不能使溴水褪色
③能发生的反应类型有:加成、取代、氧化、加聚
④它的同分异构体中可能有芳香族化合物
⑤1mol该有机物水解时只能消耗1molNaOH
⑥1mol该有机物在一定条件下和H2反应,共消耗H2为3mol.
 乙酸橙花酯是一种食用香料,其结构简式如图所示,关于该有机物的下列叙述中不正确的是( )
乙酸橙花酯是一种食用香料,其结构简式如图所示,关于该有机物的下列叙述中不正确的是( ) ①分子式为C12H20O2
②能使酸性KMnO4溶液褪色,但不能使溴水褪色
③能发生的反应类型有:加成、取代、氧化、加聚
④它的同分异构体中可能有芳香族化合物
⑤1mol该有机物水解时只能消耗1molNaOH
⑥1mol该有机物在一定条件下和H2反应,共消耗H2为3mol.
| A. | ①②③ | B. | ①②⑤ | C. | ②④⑥ | D. | ②⑤⑥ |
14.现有A、B、C、D、E五种强电解质,它们在水中可电离产生下列离子(各种离子不重复).
已知:①A、B两溶液呈碱性;C、D、E溶液呈酸性.
②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有气体产生(沉淀包括微溶物,下同).
③D溶液与另外四种溶液反应都能产生沉淀;C只能与D反应产生沉淀.试回答下列问题:
(1)分别写出B、D的化学式.B、Ba(OH)2DAgNO3;
(2)写出A、E反应的离子方程式:2Al3++3CO32-+3H2O═3CO2↑+2Al(OH)3↓;
(3)A溶液中各种离子浓度由大到小的顺序为[Na+]>[CO32-]>[OH-]>[HCO3-]>[H+]
(4)已知:NaOH( aq)+HNO3(aq)=NaNO3( aq)+H20(1)△H=-Q kJ•mol-l.写出B与C稀溶液反应的热化学方程式OH-(aq)+H+(aq)=H2O(1)△H=-QkJ/mol或$\frac{1}{2}$Ba(OH)2(aq)+HC1(aq)=$\frac{1}{2}$BaC12(aq)+H2O(1)△H=-QkJ/mol
或Ba(OH)2(aq)+2HC1(aq)=BaC12(aq)+2H2O(1)△H=-2QkJ/mol
(5)在100 mL0.1 mol•L-1 E溶液中,逐滴加入40 mL1.6 mol•L-1NaOH溶液,最终得到沉淀物质的量为0.016mol.
| 阳离子 | H+、Na+、A13+、Ag+、Ba2+ |
| 阴离子 | OH-、C1-、CO32-、NO3-、SO42- |
②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有气体产生(沉淀包括微溶物,下同).
③D溶液与另外四种溶液反应都能产生沉淀;C只能与D反应产生沉淀.试回答下列问题:
(1)分别写出B、D的化学式.B、Ba(OH)2DAgNO3;
(2)写出A、E反应的离子方程式:2Al3++3CO32-+3H2O═3CO2↑+2Al(OH)3↓;
(3)A溶液中各种离子浓度由大到小的顺序为[Na+]>[CO32-]>[OH-]>[HCO3-]>[H+]
(4)已知:NaOH( aq)+HNO3(aq)=NaNO3( aq)+H20(1)△H=-Q kJ•mol-l.写出B与C稀溶液反应的热化学方程式OH-(aq)+H+(aq)=H2O(1)△H=-QkJ/mol或$\frac{1}{2}$Ba(OH)2(aq)+HC1(aq)=$\frac{1}{2}$BaC12(aq)+H2O(1)△H=-QkJ/mol
或Ba(OH)2(aq)+2HC1(aq)=BaC12(aq)+2H2O(1)△H=-2QkJ/mol
(5)在100 mL0.1 mol•L-1 E溶液中,逐滴加入40 mL1.6 mol•L-1NaOH溶液,最终得到沉淀物质的量为0.016mol.

 实验室需要配制100mL 0.1mol•L-1 CuSO4溶液.
实验室需要配制100mL 0.1mol•L-1 CuSO4溶液.