题目内容
经测某芳香化合物A的化学式为C9H8O3,其苯环上有2个处于对位而且不含支链的取代基.反应①可能得到D1
和D2两种产物,F是E进行分子内酯化的产物,F中除苯环外还有一个四元环,各物质的关系为:
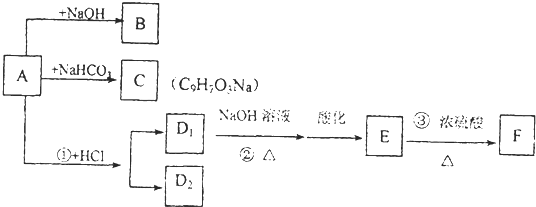
(1)写出A、C、E的结构简式:
A: ;C: ;E: ;
(2)下列有关说法正确的是 :
A.1molA与足量浓溴水反应最多可消耗4molBr2.
B.A、B遇FeCl3溶液时都能发生显色反应
C.A、C都能使紫色的酸性KMnO4溶液褪色
D.D1和D2两种物质互为同分异构体
(3)写出A→B的化学反应方程式: .
和D2两种产物,F是E进行分子内酯化的产物,F中除苯环外还有一个四元环,各物质的关系为:

(1)写出A、C、E的结构简式:
A:
(2)下列有关说法正确的是
A.1molA与足量浓溴水反应最多可消耗4molBr2.
B.A、B遇FeCl3溶液时都能发生显色反应
C.A、C都能使紫色的酸性KMnO4溶液褪色
D.D1和D2两种物质互为同分异构体
(3)写出A→B的化学反应方程式:
考点:有机物的推断
专题:有机物的化学性质及推断
分析:经测某芳香化合物A的化学式为C9H8O3,A的不饱和度=
=6,苯环的不饱和度是4,所以A的支链上还含有2个双键或一个三键,A能和碳酸氢钠溶液说明含有羧基,A能和HCl发生反应生成D1和D2,则该反应为加成反应,则说明A中含有碳碳双键,其苯环上有2个处于对位而且不含支链的取代基,结合A、C的分子式知,A的结构简式为: ,A和氢氧化钠溶液反应生成B,B的结构简式为:
,A和氢氧化钠溶液反应生成B,B的结构简式为: ,A和碳酸氢钠反应生成C,C的结构简式为
,A和碳酸氢钠反应生成C,C的结构简式为 ,A和HCl发生加成反应生成D1 、D2,
,A和HCl发生加成反应生成D1 、D2,
D1发生取代反应然后酸化生成E,F是E进行分子内酯化的产物,F中除苯环外还有一个四元环,则E的结构简式为: ,D1的结构简式为
,D1的结构简式为 ,D2的结构简式为:
,D2的结构简式为: ,F的结构简式为
,F的结构简式为 ,结合物质的结构和性质分析解答.
,结合物质的结构和性质分析解答.
| 9×2+2-8 |
| 2 |
 ,A和氢氧化钠溶液反应生成B,B的结构简式为:
,A和氢氧化钠溶液反应生成B,B的结构简式为: ,A和碳酸氢钠反应生成C,C的结构简式为
,A和碳酸氢钠反应生成C,C的结构简式为 ,A和HCl发生加成反应生成D1 、D2,
,A和HCl发生加成反应生成D1 、D2,D1发生取代反应然后酸化生成E,F是E进行分子内酯化的产物,F中除苯环外还有一个四元环,则E的结构简式为:
 ,D1的结构简式为
,D1的结构简式为 ,D2的结构简式为:
,D2的结构简式为: ,F的结构简式为
,F的结构简式为 ,结合物质的结构和性质分析解答.
,结合物质的结构和性质分析解答.解答:
解:经测某芳香化合物A的化学式为C9H8O3,A的不饱和度=
=6,苯环的不饱和度是4,所以A的支链上还含有2个双键或一个三键,A能和碳酸氢钠溶液说明含有羧基,A能和HCl发生反应生成D1和D2,则该反应为加成反应,则说明A中含有碳碳双键,其苯环上有2个处于对位而且不含支链的取代基,结合A、C的分子式知,A的结构简式为: ,A和氢氧化钠溶液反应生成B,B的结构简式为:
,A和氢氧化钠溶液反应生成B,B的结构简式为: ,A和碳酸氢钠反应生成C,C的结构简式为
,A和碳酸氢钠反应生成C,C的结构简式为 ,A和HCl发生加成反应生成D1 、D2,
,A和HCl发生加成反应生成D1 、D2,
D1发生取代反应然后酸化生成E,F是E进行分子内酯化的产物,F中除苯环外还有一个四元环,则E的结构简式为: ,D1的结构简式为
,D1的结构简式为 ,D2的结构简式为:
,D2的结构简式为: ,F的结构简式为
,F的结构简式为 ,
,
(1)通过以上分析知,A、C、E的结构简式分别为 、
、 、
、 ,
,
故答案为: 、
、 、
、 ;
;
(2)A.A的结构简式为 ,酚羟基的邻位、碳碳双键能和溴发生反应,所以1molA与足量浓溴水反应最多可消耗3molBr2,故A错误;
,酚羟基的邻位、碳碳双键能和溴发生反应,所以1molA与足量浓溴水反应最多可消耗3molBr2,故A错误;
B.A、B的结构简式分别为
 、
、 ,B中不含酚羟基,所以B不和氯化铁溶液发生显色反应,故B错误;
,B中不含酚羟基,所以B不和氯化铁溶液发生显色反应,故B错误;
C.A、C的结构简式分别为 、
、 ,都含有碳碳双键,且连接苯环的碳原子上含有氢原子,所以都能被酸性高锰酸钾溶液氧化,所以都能使酸性高锰酸钾溶液褪色,故C正确;
,都含有碳碳双键,且连接苯环的碳原子上含有氢原子,所以都能被酸性高锰酸钾溶液氧化,所以都能使酸性高锰酸钾溶液褪色,故C正确;
D.D1的结构简式为 ,D2的结构简式为:
,D2的结构简式为: ,二者的分子式相同但结构不同,所以D1和D2两种物质互为同分异构体,故D正确;
,二者的分子式相同但结构不同,所以D1和D2两种物质互为同分异构体,故D正确;
故选CD;
(3)A、B的结构简式分别为
 、
、 ,A和氢氧化钠发生中和反应,反应方程式为:
,A和氢氧化钠发生中和反应,反应方程式为: +2NaOH→
+2NaOH→ +2H2O,
+2H2O,
故答案为: +2NaOH→
+2NaOH→ +2H2O.
+2H2O.
| 9×2+2-8 |
| 2 |
 ,A和氢氧化钠溶液反应生成B,B的结构简式为:
,A和氢氧化钠溶液反应生成B,B的结构简式为: ,A和碳酸氢钠反应生成C,C的结构简式为
,A和碳酸氢钠反应生成C,C的结构简式为 ,A和HCl发生加成反应生成D1 、D2,
,A和HCl发生加成反应生成D1 、D2,D1发生取代反应然后酸化生成E,F是E进行分子内酯化的产物,F中除苯环外还有一个四元环,则E的结构简式为:
 ,D1的结构简式为
,D1的结构简式为 ,D2的结构简式为:
,D2的结构简式为: ,F的结构简式为
,F的结构简式为 ,
,(1)通过以上分析知,A、C、E的结构简式分别为
 、
、 、
、 ,
,故答案为:
 、
、 、
、 ;
;(2)A.A的结构简式为
 ,酚羟基的邻位、碳碳双键能和溴发生反应,所以1molA与足量浓溴水反应最多可消耗3molBr2,故A错误;
,酚羟基的邻位、碳碳双键能和溴发生反应,所以1molA与足量浓溴水反应最多可消耗3molBr2,故A错误;B.A、B的结构简式分别为
 、
、 ,B中不含酚羟基,所以B不和氯化铁溶液发生显色反应,故B错误;
,B中不含酚羟基,所以B不和氯化铁溶液发生显色反应,故B错误;C.A、C的结构简式分别为
 、
、 ,都含有碳碳双键,且连接苯环的碳原子上含有氢原子,所以都能被酸性高锰酸钾溶液氧化,所以都能使酸性高锰酸钾溶液褪色,故C正确;
,都含有碳碳双键,且连接苯环的碳原子上含有氢原子,所以都能被酸性高锰酸钾溶液氧化,所以都能使酸性高锰酸钾溶液褪色,故C正确;D.D1的结构简式为
 ,D2的结构简式为:
,D2的结构简式为: ,二者的分子式相同但结构不同,所以D1和D2两种物质互为同分异构体,故D正确;
,二者的分子式相同但结构不同,所以D1和D2两种物质互为同分异构体,故D正确;故选CD;
(3)A、B的结构简式分别为
 、
、 ,A和氢氧化钠发生中和反应,反应方程式为:
,A和氢氧化钠发生中和反应,反应方程式为: +2NaOH→
+2NaOH→ +2H2O,
+2H2O,故答案为:
 +2NaOH→
+2NaOH→ +2H2O.
+2H2O.
点评:本题考查了有机物的推断,根据A的分子式及A和氢氧化钠、碳酸氢钠、HCl之间的反应确定A的结构简式,再结合物质的官能团及其性质、反应条件推断物质,注意连接苯环碳原子上含有氢原子的苯的同系物、含有碳碳双键或三键的烃、醛都能被酸性高锰酸钾溶液氧化,为易错点.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A、标准状况下,0.5NA二氧化硅约为11.2 L |
| B、向1L 1 mol/L氯化铝溶液中加入足量的氨水,生成AlO2-的个数为NA |
| C、2.7克铝与足量的氢氧化钠溶液反应,失去的电子数为0.3NA |
| D、1 mol铁与足量的氯气反应,失去的电子数为2NA |
将下列溶质配制成水溶液,在溶液中既存在溶质分子,又存在溶质离子的是( )
| A、NaOH |
| B、KNO3 |
| C、HCl |
| D、CH3COOH |
能正确表示下列反应的离子方程式的是( )
| A、向碳酸氢铵溶液中滴加过量的氢氧化钠溶液:HCO3-+OH-=CO32-+H2O | ||||
| B、硝酸亚铁溶液中滴加盐酸:3Fe2++4H++NO3-=3Fe3++2H2O+NO↑ | ||||
| C、少量固体Mg(OH)2溶于饱和NH4Cl溶液中:2NH4++Mg(OH)2=2NH3?H2O+Mg2+ | ||||
D、用惰性电极电解MgCl2溶液:2Cl-+2H2O
|
 CO和H2的混合气体俗称合成气,是一种重要的工业原料气,可以在一定条件下制备甲醇,二甲醚等多种有机物.工业上利用天然气(主要成分为CH4)与水进行高温重整制备合成气.
CO和H2的混合气体俗称合成气,是一种重要的工业原料气,可以在一定条件下制备甲醇,二甲醚等多种有机物.工业上利用天然气(主要成分为CH4)与水进行高温重整制备合成气.