题目内容
12.下列物质属于电解质的是( )| A. | AgCl | B. | 硝酸钾溶液 | C. | NH3 | D. | 二氧化碳 |
分析 电解质:在水溶液中或熔融状态下能导电的化合物;例:酸、碱、盐,金属氧化物等;
非电解质:在水溶液中和熔融状态下不能导电的化合物;例:有机物,非金属氧化物等;
解答 解:A.氯化银熔融状态下能够导电的化合物,属于电解质,故A选;
B.硝酸钾溶液为混合物,不是化合物,不属于电解质,故B不选;
C.氨气本身不能电离产生自由移动离子而导电,属于非电解质,故C不选;
D.二氧化碳本身不能电离产生自由移动离子而导电,属于非电解质,故C不选;
故选:A.
点评 本题考查了电解质判断,明确电解质概念是解题关键,注意电解质必须是化合物,必须本身能够电离产生自由移动离子,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
20.如图是某学校实验室买回的硫酸试剂标签的部分内容.判断下列说法正确的是( )


| A. | 该硫酸的浓度为9.2 mol•L-1 | |
| B. | 配制480 mL 4.6 mol•L-1的稀硫酸需该H2SO4 125mL | |
| C. | 该硫酸与等体积水混合质量分数变为49% | |
| D. | 取该硫酸100 mL,则浓度变为原来的$\frac{1}{5}$ |
7.在下列各说法中,正确的是( )
| A. | △H>0表示放热反应,△H>0表示吸热反应 | |
| B. | 热化学方程式中的化学计量数只表示物质的量,可以是分数 | |
| C. | 1 mol H2SO4与1 mol Ba(OH)2反应生成BaSO4沉淀时放出的热量叫做中和热 | |
| D. | 1 mol H2与0.5 mol O2反应放出的热就是H2的燃烧热 |
17.已知SO32-+I2+H2O=SO42-+2I-+2H+.某溶液中可能含有I-、NH4+、Cu2+、SO32-,向该无色溶液中加入少量溴水,溶液仍呈无色.则下列关于该溶液组成的判断正确的是( )
| A. | 肯定不含I- | B. | 可能含有Cu2+ | C. | 一定含有SO32- | D. | 肯定不含有NH4+ |
4.下列物质中含有相同的化学键类型的是( )
| A. | NaCl、HCl、H2O、NaOH | B. | Cl2、Na2S、HCl、SO2 | ||
| C. | Na2O2、H2O2、H2O、O3 | D. | HBr、CO2、H2O、CS2 |

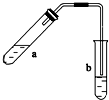 可用图示装置制取少量乙酸乙酯(部分图中均已略去).请填空:
可用图示装置制取少量乙酸乙酯(部分图中均已略去).请填空: