题目内容
脱水偶联反应是一种新型的直接烷基化反应,例如:
①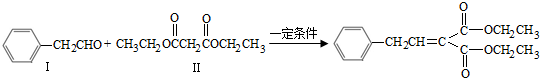
(1)化合物I的分子式为 ,1mol该物质完全燃烧最少需要消耗 mol O2
(2)化合物Ⅲ可与乙醇在浓硫酸溶液中共热生成化合物Ⅱ,相应的化学反应方程式为 .
(3)由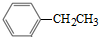 可合成化合物I.化合物Ⅳ是
可合成化合物I.化合物Ⅳ是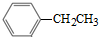 的同分异构体,Ⅳ的核磁共振氢谱有两族峰,峰面积之比为4:6,且在CrO-乙酐催化下反应生成能生成银镜反应的化合物V,Ⅳ的结构简式为 ,V的结构简式为 .
的同分异构体,Ⅳ的核磁共振氢谱有两族峰,峰面积之比为4:6,且在CrO-乙酐催化下反应生成能生成银镜反应的化合物V,Ⅳ的结构简式为 ,V的结构简式为 .
(4)一定条件下,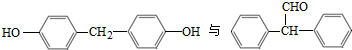 也可以发生类似反应①的反应,产物的结构式为 .
也可以发生类似反应①的反应,产物的结构式为 .
①
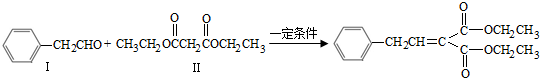
(1)化合物I的分子式为
(2)化合物Ⅲ可与乙醇在浓硫酸溶液中共热生成化合物Ⅱ,相应的化学反应方程式为
(3)由
 可合成化合物I.化合物Ⅳ是
可合成化合物I.化合物Ⅳ是 的同分异构体,Ⅳ的核磁共振氢谱有两族峰,峰面积之比为4:6,且在CrO-乙酐催化下反应生成能生成银镜反应的化合物V,Ⅳ的结构简式为
的同分异构体,Ⅳ的核磁共振氢谱有两族峰,峰面积之比为4:6,且在CrO-乙酐催化下反应生成能生成银镜反应的化合物V,Ⅳ的结构简式为(4)一定条件下,
 也可以发生类似反应①的反应,产物的结构式为
也可以发生类似反应①的反应,产物的结构式为考点:有机物分子中的官能团及其结构
专题:有机物的化学性质及推断
分析:(1)反应①中化合物I的结构简式为CH3COCH2COOCH2CH3,根据结构简式可得分子式,写出反应的方程式可得耗氧量;
(2)化合物Ⅲ可与乙醇在浓硫酸溶液中共热生成化合物Ⅱ,可以推知化合物Ⅲ的结构简式为HOOCCH2COOH,根据酯化反应的实质书写方程式;
(3)根据Ⅳ的核磁共振氢谱有两个峰,峰面积之比为4:6,可以确定结构简式,在CrO-乙酐催化下有机物的甲基能被氧化为醛基;
(4)根据反应①的特点:醛基掉氧原子,活泼的α-H掉下来,即下来小分子水后出现不饱和键的过程.
(2)化合物Ⅲ可与乙醇在浓硫酸溶液中共热生成化合物Ⅱ,可以推知化合物Ⅲ的结构简式为HOOCCH2COOH,根据酯化反应的实质书写方程式;
(3)根据Ⅳ的核磁共振氢谱有两个峰,峰面积之比为4:6,可以确定结构简式,在CrO-乙酐催化下有机物的甲基能被氧化为醛基;
(4)根据反应①的特点:醛基掉氧原子,活泼的α-H掉下来,即下来小分子水后出现不饱和键的过程.
解答:
解:(1)反应①中化合物I的结构简式为CH3COCH2COOCH2CH3,其分子式为C6H10O3;根据烃的含氧衍生物燃烧通式可得:C6H10O3+7O2
6CO2+5H2O,其中氧气与I的物质的量之比等于系数之比,则1molI完全燃烧最少需要消耗7mol O2;
故答案为:C6H10O3; 7;
(2)化合物Ⅲ可与乙醇在浓硫酸溶液中共热生成化合物Ⅱ,可以推知化合物Ⅲ的结构简式为HOOCCH2COOH,化合物Ⅲ与乙醇在浓硫酸溶液中共热生成化合物Ⅱ的化学反应方程式为2CH3CH20H+HOOCCH2COOH
 +2H2O,
+2H2O,
故答案为:2CH3CH20H+HOOCCH2COOH
 +2H2O;
+2H2O;
(3) 的同分异构体,Ⅳ的核磁共振氢谱有两族峰,峰面积之比为4:6,则Ⅳ为对二甲苯,根据信息在CrO-乙酐催化下反应生成能生成银镜反应的化合物V为
的同分异构体,Ⅳ的核磁共振氢谱有两族峰,峰面积之比为4:6,则Ⅳ为对二甲苯,根据信息在CrO-乙酐催化下反应生成能生成银镜反应的化合物V为 ,
,
故答案为: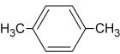 ;
; ;
;
(4) 发生类似反应①的反应产物是
发生类似反应①的反应产物是 ,
,
故答案为: .
.
| ||
故答案为:C6H10O3; 7;
(2)化合物Ⅲ可与乙醇在浓硫酸溶液中共热生成化合物Ⅱ,可以推知化合物Ⅲ的结构简式为HOOCCH2COOH,化合物Ⅲ与乙醇在浓硫酸溶液中共热生成化合物Ⅱ的化学反应方程式为2CH3CH20H+HOOCCH2COOH
| 浓硫酸 |
| △ |
 +2H2O,
+2H2O,故答案为:2CH3CH20H+HOOCCH2COOH
| 浓硫酸 |
| △ |
 +2H2O;
+2H2O;(3)
 的同分异构体,Ⅳ的核磁共振氢谱有两族峰,峰面积之比为4:6,则Ⅳ为对二甲苯,根据信息在CrO-乙酐催化下反应生成能生成银镜反应的化合物V为
的同分异构体,Ⅳ的核磁共振氢谱有两族峰,峰面积之比为4:6,则Ⅳ为对二甲苯,根据信息在CrO-乙酐催化下反应生成能生成银镜反应的化合物V为 ,
,故答案为:
 ;
; ;
;(4)
 发生类似反应①的反应产物是
发生类似反应①的反应产物是 ,
,故答案为:
 .
.
点评:本题考查考生对烯烃、炔烃、卤代烃、醇、醛、酯等常见有机物的结构和成键特征的了解;考查考生对以上有机物典型代表物的组成和性质以及它们相互联系的了解;考查考生对重要有机反应类型如取代反应、加成反应、消去反应和氧化反应的了解;考查考生对核磁共振氢谱峰组数和峰面积之比的了解;考查考生对有机化合物同分异构现象的了解;考查考生的分析能力、逻辑推理能力、综合应用信息以及信息迁移能力.

练习册系列答案
相关题目
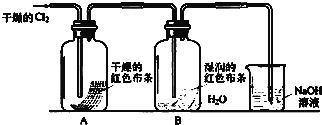


 氮是地球上含量丰富的一种元素,氨和肼(N2H4)是氮的两种常见化合物,在科学技术和生产中有重要的应用.
氮是地球上含量丰富的一种元素,氨和肼(N2H4)是氮的两种常见化合物,在科学技术和生产中有重要的应用. (1)写出实验室由苯和浓硝酸反应制取硝基苯的化学方程式:
(1)写出实验室由苯和浓硝酸反应制取硝基苯的化学方程式: