题目内容
为了探究HClO的漂白性,某同学设计了如下的实验.
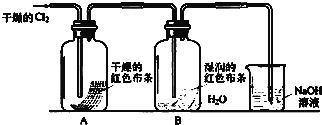
(1)通入Cl2后,集气瓶A中的现象是: ,从而得出的结论是 ;集气瓶B中的现象是: ,从而得出的结论是 ,其中发生的反应的化学方程式为 .
(2)为了确证是HClO使湿润的红色布条褪色,你认为还应增加的实验是 .
(3)烧杯中NaOH溶液所起的作用是 ,烧杯中所发生反应的化学方程式为 .

(1)通入Cl2后,集气瓶A中的现象是:
(2)为了确证是HClO使湿润的红色布条褪色,你认为还应增加的实验是
(3)烧杯中NaOH溶液所起的作用是
考点:性质实验方案的设计
专题:元素及其化合物
分析:由实验装置图可知,干燥的氯气进入A中,干燥的红色布条不褪色,B中氯气与水反应生成HClO,则布条褪色,说明干燥的氯气没有漂白性,潮湿的氯气具有漂白性;最后利用NaOH溶液吸收氯气,进行尾气处理,以此来解答.
解答:
解:(1)通入Cl2后,从集气瓶A中观察到干燥的红色布条不褪色,可得出的结论干燥的氯气没有漂白性;从集气瓶B中湿润的红色布条褪色,可得出的结论是HClO能漂白,因为氯气和水反应Cl2+H2O?HCl+HClO,生成的次氯酸具有漂白性,
故答案为:干燥的红色布条不褪色;干燥的氯气没有漂白性;湿润的红色布条褪色;氯水具有漂白性;Cl2+H2O?HCl+HClO;
(2)由Cl2+H2O?HCl+HClO可知,生成盐酸和HClO,则设计一个实验为验证HCl是否有漂白性,操作方法是在一个红色布条上滴加盐酸,布条无变化,排除氯化氢的漂白性,就证明起漂白作用的物质是次氯酸,
故答案为:验证HCl是否有漂白性;
(3)氯气有毒,不能排放在空气中,NaOH溶液所起的作用是吸收多余的氯气,氯气与氢氧化钠反应生成氯化钠、次氯酸钠和水,反应的化学方程式为2NaOH+Cl2═NaCl+NaClO+H2O,故答案为:吸收多余的氯气;2NaOH+Cl2═NaCl+NaClO+H2O.
故答案为:干燥的红色布条不褪色;干燥的氯气没有漂白性;湿润的红色布条褪色;氯水具有漂白性;Cl2+H2O?HCl+HClO;
(2)由Cl2+H2O?HCl+HClO可知,生成盐酸和HClO,则设计一个实验为验证HCl是否有漂白性,操作方法是在一个红色布条上滴加盐酸,布条无变化,排除氯化氢的漂白性,就证明起漂白作用的物质是次氯酸,
故答案为:验证HCl是否有漂白性;
(3)氯气有毒,不能排放在空气中,NaOH溶液所起的作用是吸收多余的氯气,氯气与氢氧化钠反应生成氯化钠、次氯酸钠和水,反应的化学方程式为2NaOH+Cl2═NaCl+NaClO+H2O,故答案为:吸收多余的氯气;2NaOH+Cl2═NaCl+NaClO+H2O.
点评:本题考查性质实验方案的设计,为高频考点,把握实验装置的作用、发生的反应、实验设计的分析为解答的关键,注意验证HClO具有漂白性,利用对比和排除干扰的方法来解答,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
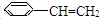 )5种有机物分别在一定条件下与H2充分反应,按下列各题要求填空
)5种有机物分别在一定条件下与H2充分反应,按下列各题要求填空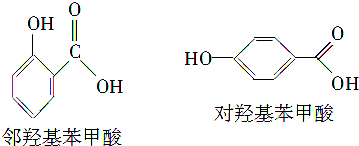
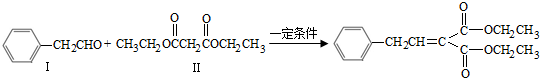
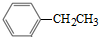 可合成化合物I.化合物Ⅳ是
可合成化合物I.化合物Ⅳ是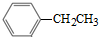 的同分异构体,Ⅳ的核磁共振氢谱有两族峰,峰面积之比为4:6,且在CrO-乙酐催化下反应生成能生成银镜反应的化合物V,Ⅳ的结构简式为
的同分异构体,Ⅳ的核磁共振氢谱有两族峰,峰面积之比为4:6,且在CrO-乙酐催化下反应生成能生成银镜反应的化合物V,Ⅳ的结构简式为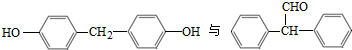 也可以发生类似反应①的反应,产物的结构式为
也可以发生类似反应①的反应,产物的结构式为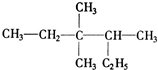 系统命名法命名为
系统命名法命名为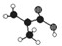 所示(图中球与球之间的连线代表化学键,如单键、双键等).
所示(图中球与球之间的连线代表化学键,如单键、双键等).