��Ŀ����
11��ij���������Ҫ�ɷ���FeCO3��������SiO2������CaCO3�� Al2O3��ͼ�����ø��������Ʊ�����Fe3O4�������ӵļ�Ҫ�������̣�
��1��������ʯ�����Ŀ����������������������������ʱ�Ļ�ѧ��Ӧ���ʣ�����ɷ��ýϱ��˵�Ca��OH��2���NaOH��˵�����ɣ����ܣ�Ca��OH��2�ܽ�Ƚ�С����˳���ܽ������е�Al2O3��
��2�����������ϡ����ɷ���ò��ӷ���ϡ���˵�����ɲ��ɣ�CaSO4�ܺ��ѳ��������е�CaCO3�����������ϡ�������������֮ǰ�������������ѧʵ������Ϊ���ˣ�
��3�����������������ӷ���ʽΪClO3-+6H++6Fe2+=Cl-+6Fe3++3H2O��
��4�����ʵ����֤����������������Һ�д���Fe2+���������еμӸ������������Һ����������Ϻ�ɫ��ȥ��˵����Һ���д�Fe2+��
��5��Fe3O4������ֱ���ķ�Χ��1��100nm��
���� ���������Ҫ�ɷ���FeCO3��������SiO2������CaCO3�� Al2O3��������������������Һ���������衢���������ܽ�������������Һ�У������ﺬ��FeCO3������CaCO3������ϡ���Ὣ̼��ƺ�̼���������룬���˺�����Һ�м���NaClO3����ʹ�������������������������ӣ�����Һ�м���̼�����ƣ��ڵ����Ļ����з�Ӧ�����������������ô���������ɵ�Fe3O4���壬�Դ˽����⣮
��� �⣺��1��������ʯ���飬����������������Ӧ���ʣ���������Ũ�Ƚϵͣ���Һ���Խ����������ܽ���������
�ʴ�Ϊ��������������������������ʱ�Ļ�ѧ��Ӧ���ʣ����ܣ�Ca��OH��2�ܽ�Ƚ�С����˳���ܽ������е�Al2O3��
��2�����ܼ���ϡ����������ᣬ������������ƣ�����ˮ�����Գ��������е�̼��ƣ�������������������˳�ȥ���ʣ�
�ʴ�Ϊ�����ɣ�CaSO4�ܺ��ѳ��������е�CaCO3�����ˣ�
��3����������������������¿����������ӣ����ӷ���ʽΪClO3-+6H++6Fe2+=Cl-+6Fe3++3H2O���ʴ�Ϊ��ClO3-+6H++6Fe2+=Cl-+6Fe3++3H2O��
��4���������Ӿ��л�ԭ�ԣ����������ط���������ԭ��Ӧ�����鷽�����������еμӸ������������Һ����������Ϻ�ɫ��ȥ��˵����Һ���д�Fe2+��
�ʴ�Ϊ���������еμӸ������������Һ����������Ϻ�ɫ��ȥ��˵����Һ���д�Fe2+��
��5��Fe3O4������ֱ���ķ�Χ��1��100nm���ʴ�Ϊ���ʴ�Ϊ��1��100nm��
���� ���⿼�����ʵ��Ʊ���Ϊ��Ƶ���㣬���ؿ���ѧ���ķ���������ʵ��������ע��������ʵ������Լ�ʵ���ԭ�����Ѷ��еȣ�

| Ԫ�ر�� | ԭ�ӽṹ��Ԫ������ |
| X | �����ڳ�����Ϊ����ɫ���壬ˮ��Һ����Ư���� |
| Y | ����������Ԫ����ԭ�Ӱ뾶��� |
| Z | �����Ľ�����������ǿ�ᷴӦ������ǿ�Ӧ |
| M | �������������۴�����Ϊ4 |
| N | N��һ������Ԫ�أ�����ȱ�ٸ�Ԫ�ػᷢ��ƶѪ��ʹ����ɫή�� ���������������һ����������д��� |
 ��
����2��д��Z������Y������������Ӧ��ˮ���ﷴӦ�����ӷ���ʽ2Al+2OH-+6H2O=2[Al��OH��4]-+3H2������2Al+2OH-+2H2O=2AlO2-+3H2������
��3��X���ʵ�ˮ��Һ��M�ij��������������Ư����д������֮�䷴Ӧ�Ļ�ѧ����ʽCl2+SO2+2H2O=H2SO4+2HCl��
��4����д���ж�Y��Z������ǿ����һ����ʵ�������Ƶļ���ǿ�������������ԣ�
��5���ڷ�ˮ�м���N��ij���α�����Һ���Եõ�һ�ֺ��ɫ��Һ�壬���Һ������μ��뺬M������������ˮ������Һֱ�������Ĺ����з����������ǣ��ȳ��ֳ�����Ȼ������ܽ⣮
��6����֪��298Kʱ����Z��������ȼ������1mol Z2O3����ʱ���ų�����1676.2kJ������N��������ȼ������1mol N3O4����ʱ���ų�����1118.4kJ����д��298Kʱ����Z������N3O4��Ӧ���Ȼ�ѧ����ʽ��8Al��s��+3Fe3O4��s��=9Fe��s��+4Al2O3��s����H=-3349.6KJ/mol��


 �ں�����ߺ�DZˮͧ�п��ù���������Ϊ��������������ͼʵ��װ�ã�ѡ���ʵ��Ļ�ѧ�Լ���ʵ����Ʒ����Ʋ���ɶԹ���������һ���ʵ�̽����
�ں�����ߺ�DZˮͧ�п��ù���������Ϊ��������������ͼʵ��װ�ã�ѡ���ʵ��Ļ�ѧ�Լ���ʵ����Ʒ����Ʋ���ɶԹ���������һ���ʵ�̽���� ����һ��ҽҩ�м��壬�������Ʊ�����Ѫҩ����ͨ����ͼ·�ߺϳɣ�
����һ��ҽҩ�м��壬�������Ʊ�����Ѫҩ����ͨ����ͼ·�ߺϳɣ�
 ��
�� ��
�� ���úϳ�·������ͼ��ʾ����ע����Ӧ��������
���úϳ�·������ͼ��ʾ����ע����Ӧ�������� ��
��
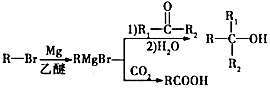
 ���䷴Ӧ����Ϊȡ����Ӧ��
���䷴Ӧ����Ϊȡ����Ӧ�� ��
�� ��д�ṹ��ʽ����
��д�ṹ��ʽ����
 ��
�� ��֪2A2��g��+B2��g��?2C3��g������H=-Q1 kJ/mol��Q1��0������һ���д����Ĺ̶��ݻ��������м���2molA2��1molB2����500��ʱ��ַ�Ӧ����ƽ���C3��Ũ��Ϊw mol•L-1���ų�����ΪQ2 kJ��
��֪2A2��g��+B2��g��?2C3��g������H=-Q1 kJ/mol��Q1��0������һ���д����Ĺ̶��ݻ��������м���2molA2��1molB2����500��ʱ��ַ�Ӧ����ƽ���C3��Ũ��Ϊw mol•L-1���ų�����ΪQ2 kJ�� ��������͵����������dz��õĻ���ԭ�ϣ���Ҳ�Ǵ�������Ҫ��Ⱦ��ۺ���������Ⱦ�ǻ�����ѧ��ǰ����Ҫ�о�����֮һ��
��������͵����������dz��õĻ���ԭ�ϣ���Ҳ�Ǵ�������Ҫ��Ⱦ��ۺ���������Ⱦ�ǻ�����ѧ��ǰ����Ҫ�о�����֮һ��