题目内容
11.下列反应的离子方程式书写正确的是( )| A. | 碳酸钙与盐酸反应:CO32-+2H+═H2O+CO2↑ | |
| B. | 稀 H2SO4与铁粉反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 氨水与稀盐酸反应:H++OH-═H2O | |
| D. | 氯化铜溶液与铁粉反应:Cu2++Fe═Fe2++Cu |
分析 A.碳酸钙为沉淀应保留化学式;
B.不符合反应客观事实;
C.一水合氨为弱碱,应保留化学式;
D.二者发生置换反应.
解答 解:A.碳酸钙与盐酸反应,离子方程式:CaCO3+2H+═H2O+CO2↑+Ca2+,故A错误;
B.稀 H2SO4与铁粉反应,离子方程式:Fe+2H+═Fe2++H2↑,故B错误;
C.氨水与稀盐酸反应,离子方程式:H++NH3•H2O═H2O+NH4+,故C错误;
D.化铜溶液与铁粉反应,离子方程式:Cu2++Fe═Fe2++Cu,故D正确;
故选:D.
点评 本题考查了离子方程式的书写,明确反应实质及离子方程式书写方法是解题关键,注意化学式的拆分,注意离子反应遵循客观事实、遵循原子个数、电荷收守恒规律,题目难度不大.

练习册系列答案
相关题目
15.已知恒容条件下,反应A2(g)+2B2(g)?2AB2(g)△H<0,下列说法正确的是( )
| A. | 升高温度,正向反应速率增加,逆向反应速率减小 | |
| B. | 达到平衡后,充入氦气,反应速率增大 | |
| C. | 达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动 | |
| D. | 达到平衡后,增大A2(g)的浓度,B2的转化率增大 |
6.下列各组离子在溶液中能大量共存,且溶液为无色的是( )
| A. | Mg2+、Na+、SO42- | B. | K+、H+、HCO3- | C. | Cu2+、NO3-、SO42- | D. | Ba2+、NO3-、CO32- |
16.用化学式填写下列空白:
由H、O、C、Fe组成的常见化合物中,属于酸性氧化物的是CO2,属于无机含氧酸的是H2CO3,属于碱的是Fe(OH)2或Fe(OH)3,属于有机物的是C2H5OH,CH4.
由H、O、C、Fe组成的常见化合物中,属于酸性氧化物的是CO2,属于无机含氧酸的是H2CO3,属于碱的是Fe(OH)2或Fe(OH)3,属于有机物的是C2H5OH,CH4.
3.用惰性电极电解一定量的硫酸铜溶液,电解过程中的实验数据如图所示.横坐标表示转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况),下列判断正确的是( )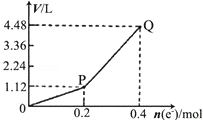

| A. | 电解过程中,溶液的pH不断增大 | |
| B. | Q点对应的气体中,H2与O2的体积比为2:1 | |
| C. | 阳极电极反应式为2H2O+4e-═4H++O2↑ | |
| D. | 当转移0.4mole-时,电解生成的铜为6.4g |
20.下列分散系能发生丁达尔效应的是( )
| A. | 泥水混合物 | B. | 食盐水 | C. | 蔗糖溶液 | D. | 烟、云、雾 |
1.下列粒子在化学反应中既能显示氧化性又能显示还原性的是( )
| A. | Al3+ | B. | Fe2+ | C. | Al | D. | Br- |
 A、B、C、D都是初中化学中的常见物质,具有如图所示的转化关系(反应条件、有些反应物或产 物已略去):
A、B、C、D都是初中化学中的常见物质,具有如图所示的转化关系(反应条件、有些反应物或产 物已略去):