题目内容
3.以下3组热化学方程式中Q1>Q2的是( )①2H2S(g)+3O2(g)=2SO2(g)+2H2O(l)△H=-Q1kJ/mol
2H2S(g)+O2(g )=2S (s)+2H2O(l)△H=-Q2kJ/mol
②H+(aq)+OH-(aq)=H2O(l)△H=-Q1kJ/mol
CH3COOH(aq)+OH-(aq)=CH3COO- (aq)+H2O(l)△H=-Q2kJ/mol
③CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-Q1kJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-Q2kJ/mol.
| A. | ①② | B. | ①②③ | C. | ②③ | D. | ② |
分析 ①完全燃烧比不完全燃烧放出的热量多;
②醋酸为弱酸,电离吸热,中和反应放热;
③反应物相同,产物中只有水的状态不同,气态水的能量高.
解答 解:①完全燃烧比不完全燃烧放出的热量多,则Q1>Q2,故选;
②醋酸为弱酸,电离吸热,中和反应放热,醋酸发生中和反应放出热量少,则Q1>Q2,故选;
③反应物相同,产物中只有水的状态不同,气态水的能量高,则生成气态水放出热量少,则Q1>Q2,故选;
故选B.
点评 本题考查反应热与焓变,为高频考点,把握反应中能量变化、焓变与热量的区别为解答的关键,侧重分析与应用能力的考查,注意物质状态及电离应用,题目难度不大.

练习册系列答案
 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
13.硝酸与金属反应往往产生氮氧化物,但是在某些特殊情况则不然.将稀硝酸(HNO3浓度低于2mol•L一1)与过量金属镁缓和反应放出一种无色无毒气体A,反应完全后向剩余溶液中加人过量NaOH固体并加热,放出气体B,将两次放出气体全部收集并混合,用碱石灰干燥后缓慢通过足量的灼热氧化铜固体,观察到固体变红,将剩余气体用浓硫酸干燥,最后气体体积变为原来的四分之三,则下列分析正确的是(本题中所有气体体积均为相同条件下测得的体积)( )
| A. | 无色无毒气体A为H2 | |
| B. | 最后气体为NH3 | |
| C. | 在镁与硝酸反应过程中还原剂与氧化剂的物质的量之比为5:1 | |
| D. | 气体A与气体B的体积比为1:1 |
14.下列溶液中,加热后颜色一定变浅的是( )
| A. | 稀氨水和酚酞溶液 | B. | 溶有SO2的品红溶液 | ||
| C. | 滴有酚酞的氢氧化钙溶液 | D. | 滴有酚酞的Na2CO3溶液 |
11.下列说法正确的是( )
| A. | 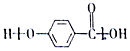 的结构中含有酯基 的结构中含有酯基 | |
| B. | 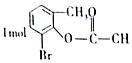 一定条件下与足量NaOH溶液反应,最多消耗3molNaOH 一定条件下与足量NaOH溶液反应,最多消耗3molNaOH | |
| C. | 按系统命名法,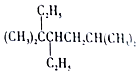 的名称为3,3,6-三甲基-4-乙基庚烷 的名称为3,3,6-三甲基-4-乙基庚烷 | |
| D. | 油脂和蛋白质都是能发生水解反应的高分子化合物 |
8.化学与材料、生活和环境密切相关,下列有关分类中正确的是( )
| A. | 新型材料聚酯纤维、光导纤维都属于有机高分子 | |
| B. | 火柴头的主要成分是氯酸钾和硫单质,分别属于电解质和非电解质 | |
| C. | 蛋白质、淀粉、纤维素都属于有机高分子化合物 | |
| D. | 天然纤维和合成纤维的主要成分是纤维素 |
13.下列反应中,改变反应物的用量、条件或浓度,不会改变生成物的是( )
| A. | 铜和硝酸反应 | B. | 二氧化碳通入氢氧化钠溶液中 | ||
| C. | 细铁丝在氯气中燃烧 | D. | 铁和与硫酸溶液反应 |