题目内容
14.下列变化属于物理变化的是( )| A. | 石油裂解 | B. | 石油的分馏 | ||
| C. | 石油的裂化 | D. | 甲烷和氯气混合后光照 |
分析 A.石油的裂解是采用较高的温度,让大分子烃类有机物成为小分子烃的过程;
B.石油分馏是根据石油中各成分的沸点不同而分离的,变化过程中没有新物质生成;
C.石油的裂化是让大分子烃类有机物成为小分子烃的过程;
D.甲烷和氯气混合后光照生成一氯甲烷和氯化氢.
解答 解:A.石油裂解是大分子分解生成小分子,是化学变化,故A错误;
B.石油分馏是根据石油中各成分的沸点不同而分离的,变化过程中没有新物质生成,属于物理变化,故B正确;
C.石油的裂化是让大分子烃类有机物成为小分子烃的过程,该过程中有新物质生成,属于化学变化,故C错误;
D.甲烷和氯气混合后光照生成一氯甲烷和氯化氢,有新物质生成,属于化学变化,故D错误.
故选B.
点评 本题考查物理变化与化学变化的区别与联系,难度不大,解答时要分析变化过程中是否有新物质生成,这里的新物质是指和变化前的物质是不同种的物质,若没有新物质生成属于物理变化,若有新物质生成属于化学变化.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
4.表是元素周期表的一部分,针对a~K十一种元素回答下列问题(请用具体化学式回答)
(1)这些元素中非金属性最强的单质是F2,最高价氧化物对应水化物酸性最强的是HClO4,最高价氧化物对应水化物碱性最强是NaOH.
(2)表中K的氢化物的化学式为H2S,它的还原性比j的氢化物还原性强(填“强”或“弱”),它水溶液的酸性比j的氢化物水溶液的酸性弱(填“强”或“弱”).
(3)e单质的电子式为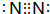 ,e的氢化物的结构式为
,e的氢化物的结构式为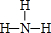 .
.
(4)用电子式表示h与k构成化合物的形成过程
(5)写出i的氧化物与强碱反应的离子方程式Al2O3+2OH-=2AlO2-+H2O
(6)H2和e的单质化合的反应是可逆反应,且该反应正方向放热.将等物质的量的H2、e的单质充入一恒容密闭容器中,在适当条件下反应.下列说法正确的是AD(填写选项).
A.升高温度,不论正反应方向还是逆反应方向速率都加快
B.向上述容器中充入适量Ar气可加快反应速率
C.反应过程中,e的单质的体积分数始终为50%
D.反应器内压强不随时间变化而变化,说明反应到达平衡.
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 2 | a | c | d | e | f | g | |
| 3 | b | h | i | j | k |
(2)表中K的氢化物的化学式为H2S,它的还原性比j的氢化物还原性强(填“强”或“弱”),它水溶液的酸性比j的氢化物水溶液的酸性弱(填“强”或“弱”).
(3)e单质的电子式为
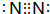 ,e的氢化物的结构式为
,e的氢化物的结构式为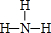 .
.(4)用电子式表示h与k构成化合物的形成过程

(5)写出i的氧化物与强碱反应的离子方程式Al2O3+2OH-=2AlO2-+H2O
(6)H2和e的单质化合的反应是可逆反应,且该反应正方向放热.将等物质的量的H2、e的单质充入一恒容密闭容器中,在适当条件下反应.下列说法正确的是AD(填写选项).
A.升高温度,不论正反应方向还是逆反应方向速率都加快
B.向上述容器中充入适量Ar气可加快反应速率
C.反应过程中,e的单质的体积分数始终为50%
D.反应器内压强不随时间变化而变化,说明反应到达平衡.
5.分枝酸结构简式如图,下列说法正确的是( )


| A. | 分子式为C10H8O6 | |
| B. | 分子中含有3种官能团 | |
| C. | 可与乙醇、乙酸反应,且反应类型相同 | |
| D. | 1mol分枝酸最多可与3mol NaOH发生中和反应 |
2.下列物质中,属于共价化合物的是( )
| A. | Cl2 | B. | NH4Cl | C. | C2H6 | D. | KOH |
9.下列有关说法正确的是( )
| A. | 铅蓄电池放电时,正极和负极的电极质量均增大 | |
| B. | 反应Cl2(g)+H2O(1)=HCl(aq)+HClO(aq)在常温下能自发进行,则该反应的△H<0 | |
| C. | 在N2(g)+3H2(g)?2NH3(g)平衡体系中加入催化剂,N2的反应速率和转化率均增大 | |
| D. | C2H5Br水解生成乙醇(△H>0),加入少量NaOH浓溶液并加热,该化学反应速率增大其平衡常数不变 |
19.乙酸乙酯在KOH溶液中水解,得到的产物是( )
| A. | 乙酸钾 | B. | 甲醇 | C. | 乙醇 | D. | 乙酸 |
6.下列关于烷烃性质的叙述正确的是( )
| A. | 烷烃分子中碳原子不可能在同一平面上 | |
| B. | 烷烃易被酸性高锰酸钾溶液氧化 | |
| C. | 在光照条件下,烷烃易与溴水发生取代反应 | |
| D. | 烷烃的卤代反应很难得到纯净的产物 |
17.某溶液中可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Fe2+和Na+.某同学为了确定其组分,设计并完成了如下实验:
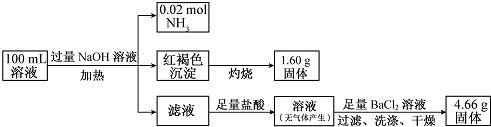
由此可推测原溶液中( )

由此可推测原溶液中( )
| A. | NH4+、Na+、SO42-一定存在,CO32--定不存在 | |
| B. | NH4+、SO42--定存在,CO32-、Na+-定不存在 | |
| C. | c(Cl-)至少为0.2 mol/L | |
| D. | c(Fe3+)一定为0.2 mol/L |
18.已知: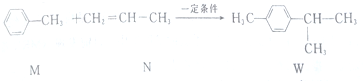 ,下列说法不正确的是( )
,下列说法不正确的是( )
 ,下列说法不正确的是( )
,下列说法不正确的是( )| A. | M的所有原子可能在同一平面上 | |
| B. | N的二氯代物有5种同分异构体(不考虑立体异构) | |
| C. | W的分子式为C10H14 | |
| D. | M、N和W均能发生氧化反应和加成反应 |