题目内容
下列反应:①Na+H2O②Na2O+H2O③NO2+H2O ④Cl2+H2O⑤F2+H2O⑥SO2+H2O中,属于氧化还原反应,但水既不是氧化剂,又不是还原剂的是( )
| A、①③ | B、②⑥ | C、③④ | D、④⑤ |
考点:氧化还原反应
专题:氧化还原反应专题
分析:有元素化合价变化的反应属于氧化还原反应,在氧化还原反应中水中H、O元素的化合价都不发生变化,则水既不作氧化剂又不作还原剂.
解答:
解:①2Na+2H2O=2NaOH+H2↑中,水中氢元素的化合价降低,则水作氧化剂,故错误;
②Na2O+H2O=2NaOH中,该反应中各元素的化合价都不变化,所以不是氧化还原反应,故错误;
③3NO2+H2O=2HNO3+NO中,二氧化氮中氮元素的化合价既有升高的又有降低的,所以二氧化氮既作氧化剂又作还原剂,而水中H、O元素的化合价都不发生变化,则水既不作做氧化剂、又不作还原剂,故正确;
④Cl2+H2O=HCl+HClO中,氯气中氯元素的化合价既有升高又有降低,所以氯气既作氧化剂又作还原剂,而水中H、O元素的化合价都不发生变化,则水既不作做氧化剂、又不作还原剂,故正确;
⑤F2和H2O的反应中F元素的化合价降低,氧元素的化合价升高,则属于氧化还原反应,且水作还原剂,故错误;
⑥SO2+H2O=H2SO3中,该反应中各元素的化合价都不变化,所以不是氧化还原反应,故错误.
故选C.
②Na2O+H2O=2NaOH中,该反应中各元素的化合价都不变化,所以不是氧化还原反应,故错误;
③3NO2+H2O=2HNO3+NO中,二氧化氮中氮元素的化合价既有升高的又有降低的,所以二氧化氮既作氧化剂又作还原剂,而水中H、O元素的化合价都不发生变化,则水既不作做氧化剂、又不作还原剂,故正确;
④Cl2+H2O=HCl+HClO中,氯气中氯元素的化合价既有升高又有降低,所以氯气既作氧化剂又作还原剂,而水中H、O元素的化合价都不发生变化,则水既不作做氧化剂、又不作还原剂,故正确;
⑤F2和H2O的反应中F元素的化合价降低,氧元素的化合价升高,则属于氧化还原反应,且水作还原剂,故错误;
⑥SO2+H2O=H2SO3中,该反应中各元素的化合价都不变化,所以不是氧化还原反应,故错误.
故选C.
点评:本题考查氧化还原反应,为高频考点,侧重于学生的分析能力的考查,明确反应中元素的化合价是解答本题的关键,难度不大,注重基础.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在pH=3的FeCl3溶液和pH=3的盐酸中,由水电离出来的H+的浓度分别为C1、C2,pH=11的Na2CO3溶液中水电离出来的OH-的浓度为C3,则它们之间的关系是( )
| A、C1<C2<C3 |
| B、C1=C3>C2 |
| C、C1>C2>C3 |
| D、无法判断 |
己烷的同分异构体共有多少种( )
| A、4 | B、5 | C、6 | D、7 |
下列各化合物的命名中不正确的是( )
| A、CH2=CH-CH=CH2 1,3-丁二烯 |
B、 3-丁醇 3-丁醇 |
C、 邻-甲基苯酚 邻-甲基苯酚 |
D、 2-甲基丁烷 2-甲基丁烷 |
依照阿伏加德罗定律,下列叙述不正确的是( )
| A、同温同压下,两种气体的体积之比等于物质的量之比 |
| B、同温同压下,两种气体的体积之比等于分子数之比 |
| C、同温同压下,两种气体的物质的量之比等于摩尔质量之比 |
| D、同温同体积下,两种气体的物质的量之比等于压强之比 |
我国科学家在世界上第一次为一种名为“钴酞菁”的分子(直径为1.3×10-9m、分子式为C32H16N8Co)恢复了磁性.已知该物质主要用于有机反应中的催化剂以及光电子等高新技术领域.下列说法中不正确的是( )
| A、“钴酞菁”分子所形成的分散系具有丁达尔效应 |
| B、该物质属于有机高分子化合物 |
| C、此项工作的研究表明,人们可以改变分子的某些物理性质 |
| D、此项研究结果可广泛应用于光电器件、生物技术等方面 |
化合物HIn在水溶液中因存在以下电离平衡,故可用作酸碱指示剂HIn(红色溶液)?H+(溶液)+In-(黄色溶液)
浓度为0.02mol?L-1的下列各溶液:
①盐酸
②石灰水
③NaCl溶液
④NaHSO4溶液
⑤NaHCO3溶液
⑥氨水,
⑦AlCl3溶液
其中能使指示剂显红色的是( )
浓度为0.02mol?L-1的下列各溶液:
①盐酸
②石灰水
③NaCl溶液
④NaHSO4溶液
⑤NaHCO3溶液
⑥氨水,
⑦AlCl3溶液
其中能使指示剂显红色的是( )
| A、②⑤⑥ | B、①④⑤ |
| C、①④⑦ | D、①④⑤⑦ |
下列离子方程式正确的是( )
| A、工业制取漂白粉:2Cl2+4OH-=2Cl-+2ClO-+2H2O | ||
B、向NaOH溶液中滴加同浓度的少量Ca(HCO3)2溶液:Ca2++HCO
| ||
| C、硫酸亚铁加过氧化氢溶液:Fe2++H2O2+2H+═Fe3++4H2O | ||
| D、铝粉与NaOH的D2O溶液反应:2Al+2OH-+2D2O═2AlO2-+3D2↑ |
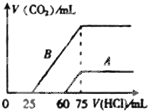 向10mL某浓度的NaOH溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同.若向M中逐滴加入0.1mol/L盐酸,产生的气体V(CO2)与加入盐酸的体积V(HCl)的关系有图示两种情况,则下列分析判断不正确的是(不考虑CO2的溶解)( )
向10mL某浓度的NaOH溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同.若向M中逐滴加入0.1mol/L盐酸,产生的气体V(CO2)与加入盐酸的体积V(HCl)的关系有图示两种情况,则下列分析判断不正确的是(不考虑CO2的溶解)( )| A、曲线A表明M中的溶质为NaOH、Na2CO3 |
| B、曲线B表明M中NaHCO3与Na2CO3的物质的量之比为1:2 |
| C、原NaOH溶液的物质的量浓度为0.75mol/L |
| D、由A.B可知,两次实验通入的CO2的体积比3:10 |