题目内容
8.常温下,在无色透明的酸性溶液中一定能大量共存的离子组是( )| A. | Na+、NH4+、SO42-、NO3- | B. | Na+、K+、SO42-、Cu2+ | ||
| C. | Ca2+、K+、Cl-、CO32- | D. | Mg2+、Fe3+、OH-、Cl- |
分析 酸性溶液中含大量的氢离子,根据离子之间不能结合生成沉淀、气体、水等,不能发生氧化还原反应等,则离子大量共存,并结合离子的颜色来解答.
解答 解:A.酸性溶液中该组离子之间不反应,可大量共存,且离子均无色,故A正确;
B.Cu2+为蓝色,与无色不符,故B错误;
C.酸溶液中不能大量存在CO32-,Ca2+、CO32-结合结合生成沉淀不能共存,故C错误;
D.Mg2+、Fe3+均与OH-反应生成沉淀,不能大量共存,且Fe3+为黄色,与无色不符,故D错误;
故选A.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意复分解反应的判断,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
16.下列叙述中正确的是( )
| A. | 以Al作阳极,Fe作阴极,AlCl3溶液作电解液,可以实现铁上镀铝 | |
| B. | 向沸水中滴加FeCl3饱和溶液制备Fe(OH)3胶体的原理是加热促进了Fe3+水解 | |
| C. | 向纯水中加入盐酸或降温,都能使水的电离平衡逆向移动,水的离子积减小 | |
| D. | 同温同压下,反应H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H相同 |
13.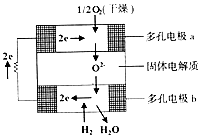 固体氧化物燃料电池是由美国西屋(West-inghouse)公司研制开发的.它以固体氧化锆一氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应.下列判断正确的是( )
固体氧化物燃料电池是由美国西屋(West-inghouse)公司研制开发的.它以固体氧化锆一氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应.下列判断正确的是( )
 固体氧化物燃料电池是由美国西屋(West-inghouse)公司研制开发的.它以固体氧化锆一氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应.下列判断正确的是( )
固体氧化物燃料电池是由美国西屋(West-inghouse)公司研制开发的.它以固体氧化锆一氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应.下列判断正确的是( )| A. | O2-向电池的正极移动 | |
| B. | 有H2放电的b极为电池的正极 | |
| C. | a极对应的电极反应为O2+2H2O+4e-=4OH- | |
| D. | 该电池的总反应方程式为2H2+O2=2H2O |
20.下列说法中不正确的是( )
| A. | Na2O2可用作呼吸面具中氧气的来源 | |
| B. | Na2O 和Na2O2投入水中都能生成NaOH | |
| C. | Na2O2和Na2O 均可以露置在空气中保存 | |
| D. | NaCl的性质稳定,可用作调味品 |
17.下列实验操作的描述中,正确的是( )
| A. | 取用Na2CO3溶液时,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中 | |
| B. | 用溶解、过滤的方法分离氯化钠和硝酸钾的混合物 | |
| C. | 称量NaOH固体,先在天平两盘上放大小相等纸片,然后NaOH放在左盘纸片上称量 | |
| D. | 利用丁达尔效应可以区别溶液和胶体 |
4.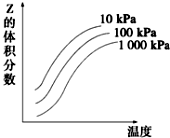 图是温度和压强对X+Y?2Z反应影响的示意图.图中横坐标表示温度,纵坐标表示平衡时混合气体中Z的体积分数.下列叙述正确的是( )
图是温度和压强对X+Y?2Z反应影响的示意图.图中横坐标表示温度,纵坐标表示平衡时混合气体中Z的体积分数.下列叙述正确的是( )
 图是温度和压强对X+Y?2Z反应影响的示意图.图中横坐标表示温度,纵坐标表示平衡时混合气体中Z的体积分数.下列叙述正确的是( )
图是温度和压强对X+Y?2Z反应影响的示意图.图中横坐标表示温度,纵坐标表示平衡时混合气体中Z的体积分数.下列叙述正确的是( )| A. | 上述可逆反应的正反应为放热反应 | B. | X、Y、Z均为气态 | ||
| C. | 增大压强平衡向正反应方向移动 | D. | 上述反应的逆反应的△H<0 |