题目内容
标准状况下,14g N2所占有的体积为 含有 个电子.
考点:气体摩尔体积
专题:阿伏加德罗常数和阿伏加德罗定律
分析:根据n=
计算出标况下氮气的物质的量,然后根据V=n?Vm计算出氮气的体积;结合1molN2中含14nol电子来计算含有的电子的物质的量,再根据N=n?NA来计算电子的数目.
| m |
| M |
解答:
解:14g N2的物质的量n=
=
=0.5mol,在标况下的体积V=n?Vm=0.5mol×22.4L/mol=11.2L;
由于1molN2中含14nol电子,故0.5molN2中含电子7mol,电子的个数N=n?NA=7mol×NA/mol=7NA,
故答案为:11.2L;7NA.
| m |
| M |
| 14g |
| 28g/mol |
由于1molN2中含14nol电子,故0.5molN2中含电子7mol,电子的个数N=n?NA=7mol×NA/mol=7NA,
故答案为:11.2L;7NA.
点评:本题考查了物质的量和体积的相关计算,掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
下列有关一定物质的量浓度的溶液配制的过程中,造成所得的溶液浓度偏大的是( )
| A、要配制100mL 1mol/L NaOH溶液,需在白纸上称4g NaOH固体,并且称量速度较慢 |
| B、称量时托盘天平的砝码已被锈蚀 |
| C、溶解或稀释溶质时烧杯尚未干燥 |
| D、定容时盖上瓶盖,摇匀后发现液面低于刻度线,再继续滴加蒸馏水使液面重新达到刻度线 |
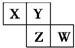 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Y原子的最外层电子数是其电子层数的3倍.下列说法正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Y原子的最外层电子数是其电子层数的3倍.下列说法正确的是( )| A、元素Y和元素Z的氢化物中均只存在极性共价键 |
| B、单核阴离子半径的大小顺序为:r(W)>r(Y)>r(Z) |
| C、元素W的最高价氧化物对应水化物的酸性最强 |
| D、元素Y和元素Z的最高正化合价相同 |
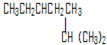 .
.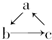 (“→”表示一步完成)关系转化的是( )
(“→”表示一步完成)关系转化的是( )