题目内容
关于焰色反应的叙述正确的是( )
| A、所有金属及其化合物在灼烧时都呈特征颜色 |
| B、进行焰色实验的铂丝用稀硫酸洗净后再蘸取样品灼烧 |
| C、透过蓝色钴玻璃观察钾元素的焰色是为了滤去黄光干扰 |
| D、金属钠在空气中燃烧发出黄光不是钠元素的焰色所致 |
考点:焰色反应
专题:金属概论与碱元素
分析:焰色反应是金属元素的一种性质,是某些金属或它们的化合物在无色火焰中灼烧时使火焰呈现特征的颜色的反应;一般用铂丝蘸取待测溶液或物质,放在火焰上灼烧,实验结束后铂丝要用稀盐酸洗涤,不同的金属元素呈现出不同的焰色反应,钾的焰色反应呈紫色(透过蓝色的钴玻璃).
解答:
解:A.焰色反应是元素的性质,只有某些金属或其化合物才有焰色反应,如Fe不具有焰色反应,故A错误;
B.进行焰色实验的铂丝用稀盐酸洗净后再灼烧至跟酒精灯火焰颜色相同后再使用,故B错误;
C.透过蓝色钴玻璃观察钾元素焰色反应的颜色为紫色,可排除钠元素黄色火焰的干扰,故C正确;
D.金属钠在空气中燃烧发出黄光是钠元素的焰色所致,故D错误;
故选C.
B.进行焰色实验的铂丝用稀盐酸洗净后再灼烧至跟酒精灯火焰颜色相同后再使用,故B错误;
C.透过蓝色钴玻璃观察钾元素焰色反应的颜色为紫色,可排除钠元素黄色火焰的干扰,故C正确;
D.金属钠在空气中燃烧发出黄光是钠元素的焰色所致,故D错误;
故选C.
点评:本题考查了焰色反应,题目难度不大,注意掌握焰色反应的步骤以及常见金属元素焰色反应的颜色.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列有关一定物质的量浓度的溶液配制的过程中,造成所得的溶液浓度偏大的是( )
| A、要配制100mL 1mol/L NaOH溶液,需在白纸上称4g NaOH固体,并且称量速度较慢 |
| B、称量时托盘天平的砝码已被锈蚀 |
| C、溶解或稀释溶质时烧杯尚未干燥 |
| D、定容时盖上瓶盖,摇匀后发现液面低于刻度线,再继续滴加蒸馏水使液面重新达到刻度线 |
常温下,不能区别浓硫酸、稀硫酸的方法是( )
| A、分别加入铁片 |
| B、分别加入蔗糖 |
| C、分别滴在纸上 |
| D、分别加入铜片 |
相同条件下,分别向等体积、pH=2的盐酸、硫酸、醋酸溶液中加入足量的Zn充分反应后产生H2的量是( )
| A、盐酸中放出的H2最多 |
| B、硫酸中放出的H2最多 |
| C、醋酸中放出的H2最多 |
| D、三种酸中产生的H2一样多 |
对于下列常见化学物质的用途认识错误的是( )
| A、明矾可用作净水剂 |
| B、干冰能用于制冷剂 |
| C、过氧化钠可以漂白任何有色物质 |
| D、小苏打是一种膨松剂,可用于制作馒头和面包 |
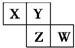 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Y原子的最外层电子数是其电子层数的3倍.下列说法正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Y原子的最外层电子数是其电子层数的3倍.下列说法正确的是( )| A、元素Y和元素Z的氢化物中均只存在极性共价键 |
| B、单核阴离子半径的大小顺序为:r(W)>r(Y)>r(Z) |
| C、元素W的最高价氧化物对应水化物的酸性最强 |
| D、元素Y和元素Z的最高正化合价相同 |
随着科学技术的不断进步,制备、研究物质的手段和途径越来越先进,H3、O4、C60、N
等相继被发现.下列有关说法中,正确的是( )
+ 5 |
| A、H2与H3互为同位素 | ||
B、N
| ||
| C、C60的硬度比金刚石大 | ||
| D、O2与O4互为同素异形体 |
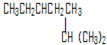 .
.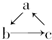 (“→”表示一步完成)关系转化的是( )
(“→”表示一步完成)关系转化的是( )