题目内容
5.NA表示阿伏伽德罗常数的数值,下列判断正确的是( )| A. | 25℃时,pH=13的NaOH溶液中含有OH-的数目为0.1NA | |
| B. | 常温下,21gC3H6和C4H8的混合物中含有的碳原子数为1.5NA | |
| C. | 46g乙醇中含有C-H键的数目为6NA | |
| D. | 常温下,2.7g金属铝与足量浓度为18mol/L的浓硫酸反应时转移的电子数为0.3NA |
分析 A、溶液体积不明确;
B、C3H6和C4H8的最简式均为CH2;
C、求出乙醇的物质的量,然后根据1mol乙醇中含5molC-H键来分析;
D、常温下铝在浓硫酸中会钝化.
解答 解:A、溶液体积不明确,故溶液中的氢氧根的个数无法计算,故A错误;
B、C3H6和C4H8的最简式均为CH2,故21g混合物中含有的CH2的物质的量为n=$\frac{21g}{14g/mol}$=1.5mol,故含1.5mol碳原子即1.5NA个,故B正确;
C、46g乙醇的物质的量为n=$\frac{46g}{46g/mol}$=1mol,而1mol乙醇中含5molC-H键,即5NA个,故C错误;
D、常温下铝在浓硫酸中会钝化,故转移的电子数小于0.3NA个,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目
16.氟是卤族元素之-,由于氟的特殊化学性质,氟化学在化学发展史上有重要的地位.下列有关说法正确的是( )
| A. | 氟原子的结构示意图: | B. | 塑料王聚四氟乙烯的结构简式: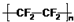 | ||
| C. | 中子数为10的氟原子:${\;}_{9}^{19}$F | D. | 萤石主要成分CaF2电子式: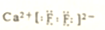 |
20.将20g铁粉放入一定量的稀硝酸中,充分反应后,放出2.24L(标准状况)NO气体,铁粉有剩余,则剩余的铁粉的质量是( )
| A. | 14.4 g | B. | 11.6 g | C. | 8.8 g | D. | 3.2 g |
10.硅酸铜钡是当今用最新科学技术才能合成的一种物质.然而现在发现,我国秦朝兵马俑用的一种颜料竟是硅酸铜钡.下列关于硅酸铜钡的学说错误的是( )
| A. | 易溶于水 | B. | 难溶于水 | C. | 属于硅酸盐 | D. | 有颜色 |
17.有关化学键及化合物的说法中,正确的是( )
| A. | 化学键是分子内原子间的相互作用 | |
| B. | 含有阴离子的化合物一定含有阳离子 | |
| C. | 离子化合物熔点一定比共价化合物高 | |
| D. | 非金属元素组成的一定是共价化合物 |
15.用NA表示阿伏加德罗常数的值.下列判断正确的是( )
| A. | 44g CO2含有的原子数目为NA | |
| B. | 常温常压下,22.4L CCl4含有的分子数目为NA | |
| C. | 32gCu与足量浓硝酸充分反应,转移电子数目为NA | |
| D. | 1mol•L-1CuSO4溶液中含有的硫酸根离子数目为NA |
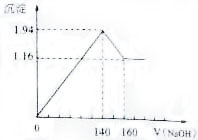 将一定质量的镁铝合金投入100mL一定浓度的盐酸中,合金完全溶解.向所得溶液中滴加浓度为0.5 mol/L的NaOH溶液,生成的沉淀质量跟加入的NaOH溶液的体积关系如图.(横坐标体积单位是mL,纵坐标质量单位是g)求:(1)合金中Mg,Al的质量;
将一定质量的镁铝合金投入100mL一定浓度的盐酸中,合金完全溶解.向所得溶液中滴加浓度为0.5 mol/L的NaOH溶液,生成的沉淀质量跟加入的NaOH溶液的体积关系如图.(横坐标体积单位是mL,纵坐标质量单位是g)求:(1)合金中Mg,Al的质量;