题目内容
艾多昔芬(Iodoxifene)是选择性雌激素受体调节剂,主要用于防治骨质疏松症和乳腺癌,其合成路线如图(部分反应条件略去):
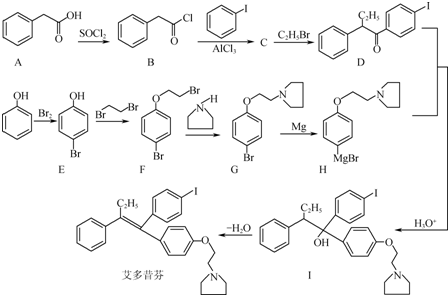
(1)化合物I中含氧官能团的名称是 、 .
(2)写出F→G的化学反应方程式: .
(3)有机物C的结构简式为 .
(4)写出同时满足下列条件的A的同分异构体的结构简式: .
①能发生银镜反应;②分子的核磁共振氢谱图中有4个峰;③能发生水解反应且产物之一遇FeCl3溶液能发生显色反应.
(5)写出以甲苯和乙酸为原料制备有机物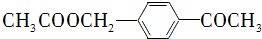 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C═CH2
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C═CH2
CH3CH2Br
CH3CH2OH.

(1)化合物I中含氧官能团的名称是
(2)写出F→G的化学反应方程式:
(3)有机物C的结构简式为
(4)写出同时满足下列条件的A的同分异构体的结构简式:
①能发生银镜反应;②分子的核磁共振氢谱图中有4个峰;③能发生水解反应且产物之一遇FeCl3溶液能发生显色反应.
(5)写出以甲苯和乙酸为原料制备有机物
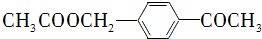 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C═CH2
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C═CH2| HBr |
| NaOH溶液 |
| △ |
考点:有机物的合成
专题:有机物的化学性质及推断
分析:根据题中各物质转化关系,对照各物质中官能团的变化及碳链结构的变化分析,
(1)根据I的结构简式可知,I中含有羟基和醚键,据此答题;
(2)比较F和G两种物质的结构简式可以写出化学方程式;
(3)比较B、D两种物质的结构及它们之间两步反应的条件可知C的结构简式;
(4)根据①能发生银镜反应,说明有醛基;②分子的核磁共振氢谱图中有4个峰;③能发生水解反应且产物之一遇FeCl3溶液能发生显色反应,说明水解产物之一有酚羟基,据此写同分异构体;
(5)以甲苯和乙酸为原料制备有机物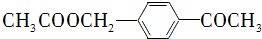 ,先将乙酸生成CH3COCl,可能参照题中A→B的过程,再在甲苯的对位上引入-COCH3基团,可以参照题中合成路线中的B→C的过程,得到
,先将乙酸生成CH3COCl,可能参照题中A→B的过程,再在甲苯的对位上引入-COCH3基团,可以参照题中合成路线中的B→C的过程,得到 ,再在甲基上卤代、碱性水解引入羟基、再与乙酸酯化得
,再在甲基上卤代、碱性水解引入羟基、再与乙酸酯化得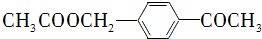 ,据此设计合成路线;
,据此设计合成路线;
(1)根据I的结构简式可知,I中含有羟基和醚键,据此答题;
(2)比较F和G两种物质的结构简式可以写出化学方程式;
(3)比较B、D两种物质的结构及它们之间两步反应的条件可知C的结构简式;
(4)根据①能发生银镜反应,说明有醛基;②分子的核磁共振氢谱图中有4个峰;③能发生水解反应且产物之一遇FeCl3溶液能发生显色反应,说明水解产物之一有酚羟基,据此写同分异构体;
(5)以甲苯和乙酸为原料制备有机物
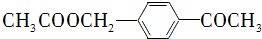 ,先将乙酸生成CH3COCl,可能参照题中A→B的过程,再在甲苯的对位上引入-COCH3基团,可以参照题中合成路线中的B→C的过程,得到
,先将乙酸生成CH3COCl,可能参照题中A→B的过程,再在甲苯的对位上引入-COCH3基团,可以参照题中合成路线中的B→C的过程,得到 ,再在甲基上卤代、碱性水解引入羟基、再与乙酸酯化得
,再在甲基上卤代、碱性水解引入羟基、再与乙酸酯化得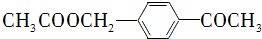 ,据此设计合成路线;
,据此设计合成路线;解答:
解:(1)根据I的结构简式可知,I中含有羟基和醚键,
故答案为:羟基、醚键;
(2)比较F和G两种物质的结构简式可以写出F→G的化学方程式为 +HBr,
+HBr,
故答案为: +HBr;
+HBr;
(3)比较B、D两种物质的结构及它们之间两步反应的条件可知,B→C的反应为B中的氯原子与碘苯中碘的对位氢原子结合,而被碘苯基团取代,所以C的结构简式为 ,
,
故答案为: ;
;
(4)根据①能发生银镜反应,说明有醛基;②分子的核磁共振氢谱图中有4个峰;③能发生水解反应且产物之一遇FeCl3溶液能发生显色反应,说明水解产物之一有酚羟基,符合这些条件的同分异构体是 ,
,
故答案为: ;
;
(5)以甲苯和乙酸为原料制备有机物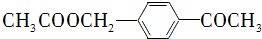 ,先将乙酸生成CH3COCl,可能参照题中A→B的过程,再在甲苯的对位上引入-COCH3基团,可以参照题中合成路线中的B→C的过程,得到
,先将乙酸生成CH3COCl,可能参照题中A→B的过程,再在甲苯的对位上引入-COCH3基团,可以参照题中合成路线中的B→C的过程,得到 ,再在甲基上卤代、碱性水解引入羟基、再与乙酸酯化得
,再在甲基上卤代、碱性水解引入羟基、再与乙酸酯化得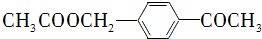 ,据此设计合成路线为
,据此设计合成路线为 ,
,
故答案为: ;
;
故答案为:羟基、醚键;
(2)比较F和G两种物质的结构简式可以写出F→G的化学方程式为
 +HBr,
+HBr,故答案为:
 +HBr;
+HBr;(3)比较B、D两种物质的结构及它们之间两步反应的条件可知,B→C的反应为B中的氯原子与碘苯中碘的对位氢原子结合,而被碘苯基团取代,所以C的结构简式为
 ,
,故答案为:
 ;
;(4)根据①能发生银镜反应,说明有醛基;②分子的核磁共振氢谱图中有4个峰;③能发生水解反应且产物之一遇FeCl3溶液能发生显色反应,说明水解产物之一有酚羟基,符合这些条件的同分异构体是
 ,
,故答案为:
 ;
;(5)以甲苯和乙酸为原料制备有机物
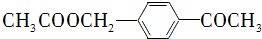 ,先将乙酸生成CH3COCl,可能参照题中A→B的过程,再在甲苯的对位上引入-COCH3基团,可以参照题中合成路线中的B→C的过程,得到
,先将乙酸生成CH3COCl,可能参照题中A→B的过程,再在甲苯的对位上引入-COCH3基团,可以参照题中合成路线中的B→C的过程,得到 ,再在甲基上卤代、碱性水解引入羟基、再与乙酸酯化得
,再在甲基上卤代、碱性水解引入羟基、再与乙酸酯化得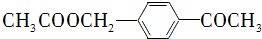 ,据此设计合成路线为
,据此设计合成路线为 ,
,故答案为:
 ;
;
点评:本题主要考查了有机物之间的相互转化和有机物的性质,难度中等,答题时注意有机官能团性质的灵活应用以及和题信息相结合进行物质推断,本题的难点是第(5)问,综合性较强,对学生综合分析问题的能力较高.

练习册系列答案
相关题目
保护地下钢管不受腐蚀,可使它连接( )
| A、铜板 | B、石墨 |
| C、直流电源负极 | D、直流电源正极 |




 +RCl→
+RCl→ +NaCl
+NaCl
 ).
).


 有多种同分异构体,写出符合下列条件的所有同分异构体的结构简式:
有多种同分异构体,写出符合下列条件的所有同分异构体的结构简式: