题目内容
Ⅰ.硅是信息产业、太阳能电池光电转化的基础材料.锌还原四氯化硅是一种有着良好应用前景的制备硅的方法,该制备过程示意图如图:

(1)焦炭在过程Ⅰ中做 剂.
(2)过程Ⅱ中Cl2用电解饱和食盐水制备,制备Cl2的化学方程式为 .
(3)整过生产过程必须严格控制无水.
①SiCl4遇水剧烈水解生成SiO2和一种酸,反应方程式为 .
②干燥Cl2时从有利于充分干燥和操作安全的角度考虑,需将约90℃的潮湿氯气先冷却至12℃,然后再通入浓H2SO4中.冷却的作用是 .
(4)Zn还原SiCl4的反应如下:
反应①:400℃~756℃,SiCl4(g)+2Zn(l)?Si(S)+2ZnCl2(l)△H1<0
反应②:756℃~907℃,SiCl4(g)+2Zn(l)?Si(S)+2ZnCl2(g)△H2<0
反应③:907℃~1410℃,SiCl4(g)+2Zn(g)?Si(S)+2ZnCl2(g)△H3<0
i.反应②的平衡常数表达式为 .
ii.对于上述三个反应,下列说明合理的是 .
a.升高温度会提高SiCl4的转化率 b.还原过程需在无氧的气氛中进行
c.增大压强能提高反应速率 d.Na、Mg可以代替Zn还原SiCl4.
(5)用硅制作太阳能电池时,为减弱光在硅表面的反射,可用化学腐蚀法在其表面形成粗糙的多孔硅层.腐蚀剂常用稀HNO3和HF的混合液.硅表面首先形成SiO2,最后转化成H2SiF6.用化学方程式表示SiO2转化为H2SiF6的过程 .
Ⅱ.(1)甲烷、氢气、一氧化碳的燃烧热分别为a kJ?mol-1,b kJ?mol-1,c kJ?mol-1,工业上利用天燃气和二氧化碳反应制备合成气(CO、H2),其热化学反应方程式为 .
(2)已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.5×10-16,Ksp(Ag2CrO4)=2.0×10-12,三种难溶盐的饱和溶液中,Ag+浓度大小的顺序为 .

(1)焦炭在过程Ⅰ中做
(2)过程Ⅱ中Cl2用电解饱和食盐水制备,制备Cl2的化学方程式为
(3)整过生产过程必须严格控制无水.
①SiCl4遇水剧烈水解生成SiO2和一种酸,反应方程式为
②干燥Cl2时从有利于充分干燥和操作安全的角度考虑,需将约90℃的潮湿氯气先冷却至12℃,然后再通入浓H2SO4中.冷却的作用是
(4)Zn还原SiCl4的反应如下:
反应①:400℃~756℃,SiCl4(g)+2Zn(l)?Si(S)+2ZnCl2(l)△H1<0
反应②:756℃~907℃,SiCl4(g)+2Zn(l)?Si(S)+2ZnCl2(g)△H2<0
反应③:907℃~1410℃,SiCl4(g)+2Zn(g)?Si(S)+2ZnCl2(g)△H3<0
i.反应②的平衡常数表达式为
ii.对于上述三个反应,下列说明合理的是
a.升高温度会提高SiCl4的转化率 b.还原过程需在无氧的气氛中进行
c.增大压强能提高反应速率 d.Na、Mg可以代替Zn还原SiCl4.
(5)用硅制作太阳能电池时,为减弱光在硅表面的反射,可用化学腐蚀法在其表面形成粗糙的多孔硅层.腐蚀剂常用稀HNO3和HF的混合液.硅表面首先形成SiO2,最后转化成H2SiF6.用化学方程式表示SiO2转化为H2SiF6的过程
Ⅱ.(1)甲烷、氢气、一氧化碳的燃烧热分别为a kJ?mol-1,b kJ?mol-1,c kJ?mol-1,工业上利用天燃气和二氧化碳反应制备合成气(CO、H2),其热化学反应方程式为
(2)已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.5×10-16,Ksp(Ag2CrO4)=2.0×10-12,三种难溶盐的饱和溶液中,Ag+浓度大小的顺序为
考点:制备实验方案的设计,热化学方程式,化学平衡常数的含义,化学平衡的影响因素,难溶电解质的溶解平衡及沉淀转化的本质
专题:基本概念与基本理论
分析:I.(1)依据碳与二氧化硅反应中元素化合价变化判断;
(2)电解氯化钠溶液生成氢氧化钠、氯气和氢气;
(3)依据反应中原子个数守恒,结合产物性质写方程式;
(4)i.K=生成物浓度幂之积与反应物浓度幂之积之比;
ii.反应2与反应1比较,反应2产物为固体和气体比反应1更易于分离,反应3与反应2比较,温度高,反应速率更快;
(5)氟化氢跟二氧化硅反应生成四氟化硅和水,四氟化硅和氟化氢直接反应生成H2SiF6;
II.(1)根据甲烷、氢气、一氧化碳的燃烧热分先书写热方程式,再利用盖斯定律来分析天燃气和二氧化碳反应制备合成气(CO、H2)的热化学方程式;
(2)据对应化学式相似的AgCl和AgI来说Ksp越小Ag+浓度越小,即AgCl>AgI;假设Ag2CrO4饱和溶液中Ag+的浓度为x,则CrO42-的浓度为0.5x,由溶度积常数的表达式计算比较即可.
(2)电解氯化钠溶液生成氢氧化钠、氯气和氢气;
(3)依据反应中原子个数守恒,结合产物性质写方程式;
(4)i.K=生成物浓度幂之积与反应物浓度幂之积之比;
ii.反应2与反应1比较,反应2产物为固体和气体比反应1更易于分离,反应3与反应2比较,温度高,反应速率更快;
(5)氟化氢跟二氧化硅反应生成四氟化硅和水,四氟化硅和氟化氢直接反应生成H2SiF6;
II.(1)根据甲烷、氢气、一氧化碳的燃烧热分先书写热方程式,再利用盖斯定律来分析天燃气和二氧化碳反应制备合成气(CO、H2)的热化学方程式;
(2)据对应化学式相似的AgCl和AgI来说Ksp越小Ag+浓度越小,即AgCl>AgI;假设Ag2CrO4饱和溶液中Ag+的浓度为x,则CrO42-的浓度为0.5x,由溶度积常数的表达式计算比较即可.
解答:
解:I.(1)碳与二氧化硅反应方程式为SiO2+2C
Si+2CO↑,碳元素在反应中化合价升高,发生氧化反应,碳做还原剂,故答案为:还原;
(2)电解氯化钠溶液生成氢氧化钠、氯气和氢气,方程式为:2NaCl+2H2O
2NaOH+Cl2↑+H2↑,故答案为:2NaCl+2H2O
2NaOH+Cl2↑+H2↑;
(3)根据SiCl4遇水剧烈水解生成SiO2和一种酸信息,反应物是SiCl4和水,生成物为二氧化硅,根据氧原子守恒,水分子前的系数为2,根据氢原子和氯原子守恒,另一产物为氯化氢,氯化氢前的系数为4,化学反应方程式为SiCl4+2H2O═SiO2+4HCl,故答案为:SiCl4+2H2O═SiO2+4HCl;
(4)i.SiCl4(g)+2Zn(l)═Si(S)+2ZnCl2(g)平衡常数表达式为:K=
,故答案为:K=
;
ii.①对于三个反应,反应热都是△H<0表示放热,
a.升高温度,平衡向吸热的方向移动,所以会降低SiCl4的转化率,故a错误;
b.Si遇氧气在高温的条件下反应生成二氧化硅,所以还原过程需在无氧的气氛中进行,b正确;
c.有气体参加的反应,增大压强,能加快反应的速率,对于三个反应,都有气体参与,所以增大压强,能提高反应的速率,故c正确;
d.Na、Mg都是还原性比较强的金属,可以代替Zn还原SiCl4,故d正确;
故答案为:bcd;
(5)二氧化硅和氢氟酸:SiO2+4HF=SiF4↑+2H2O;SiF4+2HF=H2SiF6,所以用稀HNO3和HF的混合液,硅表面首先形成SiO2,最后转化为H2SiF6的化学方程式为SiO2+6HF═H2SiF6+2H2O,故答案为:SiO2+6HF═H2SiF6+2H2O;
II.(1)甲烷、氢气、一氧化碳的燃烧热分别为akJ?mol-1,bkJ?mol-1,ckJ?mol-1,则
①CO(g)+
O2(g)=CO2(g)△H=-ckJ?mol-1
②CH4(l)+2O2(g)=CO2(g)+2 H2O(l)△H=-akJ?mol-1
③H2(g)+
O2(g)=H2O(l)△H=-bkJ?mol-1
由盖斯定律可知用②-①×2-③×2得反应CH4(l)+CO2(g)=2CO(g)+2H2(g),
该反应的反应热△H=-akJ?mol-1-(-2c)kJ?mol-1-(-2bkJ?mol-1)=-(a-2b-2c)kJ?mol-1,
故答案为:CH4(l)+CO2(g)=2CO(g)+2H2(g)△H=-(a-2b-2c)kJ?mol-1;
(2)根据对应化学式相似的AgCl和AgI来说Ksp越小Ag+浓度越小,即AgCl>AgI;假设Ag2CrO4饱和溶液中Ag+的浓度为x,则CrO42-的浓度为0.5x,由溶度积常数的表达式可知Ksp(Ag2CrO4)=x2×0.5x=0.5x3=2.0×10-12,x3=4.0×10-12,即x═
,因为AgCl饱和溶液中Ag+的浓度为
,所以Ag2CrO4>AgCl,故顺序为:Ag2CrO4>AgCl>AgI,故答案为:Ag2CrO4>AgCl>AgI.
| ||
(2)电解氯化钠溶液生成氢氧化钠、氯气和氢气,方程式为:2NaCl+2H2O
| ||
| ||
(3)根据SiCl4遇水剧烈水解生成SiO2和一种酸信息,反应物是SiCl4和水,生成物为二氧化硅,根据氧原子守恒,水分子前的系数为2,根据氢原子和氯原子守恒,另一产物为氯化氢,氯化氢前的系数为4,化学反应方程式为SiCl4+2H2O═SiO2+4HCl,故答案为:SiCl4+2H2O═SiO2+4HCl;
(4)i.SiCl4(g)+2Zn(l)═Si(S)+2ZnCl2(g)平衡常数表达式为:K=
| c2(ZnCl2) |
| c(SiCl4) |
| c2(ZnCl2) |
| c(SiCl4) |
ii.①对于三个反应,反应热都是△H<0表示放热,
a.升高温度,平衡向吸热的方向移动,所以会降低SiCl4的转化率,故a错误;
b.Si遇氧气在高温的条件下反应生成二氧化硅,所以还原过程需在无氧的气氛中进行,b正确;
c.有气体参加的反应,增大压强,能加快反应的速率,对于三个反应,都有气体参与,所以增大压强,能提高反应的速率,故c正确;
d.Na、Mg都是还原性比较强的金属,可以代替Zn还原SiCl4,故d正确;
故答案为:bcd;
(5)二氧化硅和氢氟酸:SiO2+4HF=SiF4↑+2H2O;SiF4+2HF=H2SiF6,所以用稀HNO3和HF的混合液,硅表面首先形成SiO2,最后转化为H2SiF6的化学方程式为SiO2+6HF═H2SiF6+2H2O,故答案为:SiO2+6HF═H2SiF6+2H2O;
II.(1)甲烷、氢气、一氧化碳的燃烧热分别为akJ?mol-1,bkJ?mol-1,ckJ?mol-1,则
①CO(g)+
| 1 |
| 2 |
②CH4(l)+2O2(g)=CO2(g)+2 H2O(l)△H=-akJ?mol-1
③H2(g)+
| 1 |
| 2 |
由盖斯定律可知用②-①×2-③×2得反应CH4(l)+CO2(g)=2CO(g)+2H2(g),
该反应的反应热△H=-akJ?mol-1-(-2c)kJ?mol-1-(-2bkJ?mol-1)=-(a-2b-2c)kJ?mol-1,
故答案为:CH4(l)+CO2(g)=2CO(g)+2H2(g)△H=-(a-2b-2c)kJ?mol-1;
(2)根据对应化学式相似的AgCl和AgI来说Ksp越小Ag+浓度越小,即AgCl>AgI;假设Ag2CrO4饱和溶液中Ag+的浓度为x,则CrO42-的浓度为0.5x,由溶度积常数的表达式可知Ksp(Ag2CrO4)=x2×0.5x=0.5x3=2.0×10-12,x3=4.0×10-12,即x═
| 3 | 4.0×10-12 |
| 1.8×10-10 |
点评:本题考查了硅的制备方案设计、硅及其化合物的性质及化学平衡相关知识、盖斯定律的应用、溶度积的有关计算等,掌握平衡移动原理的运用,掌握硅及其化合物的性质是解答的关键,难度中等,侧重于考查学生的实验能力和对基础知识的综合应用能力.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
只能用焰色反应实验区分的是( )
| A、钠和铜 |
| B、NaCl和K2S04 |
| C、NaCl和Na2C03 |
| D、KCl和NaCl |

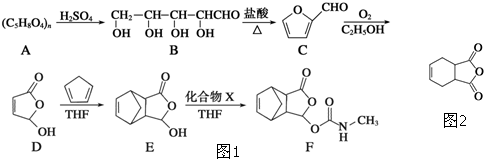
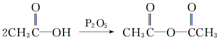 化合物G(结构如图2所示)是合成抗病毒药阿昔洛韦的中间体.请写出以OHCCH(Br)CH2CHO和1,3-丁二烯为原料制备G的合成路线流程图2(无机试剂任用).合成路线流程图示例如下:H2C=CH2
化合物G(结构如图2所示)是合成抗病毒药阿昔洛韦的中间体.请写出以OHCCH(Br)CH2CHO和1,3-丁二烯为原料制备G的合成路线流程图2(无机试剂任用).合成路线流程图示例如下:H2C=CH2
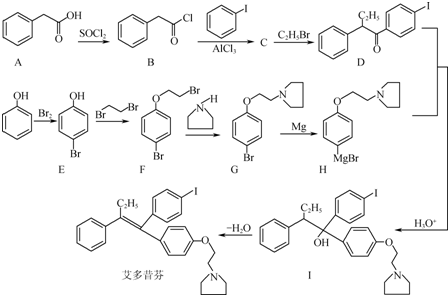
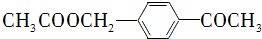 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C═CH2
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C═CH2