题目内容
过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等.某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过氧化氢的性质.
Ⅰ.测定过氧化的含量
请填写下列空白:
(1)移取10.00mL密度为ρ g/mL的过氧化氢溶液至250mL容量瓶中,加水稀释至刻度,摇匀.移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样.
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在横线上.
MnO4-+ H2O2+ H+= Mn2++ H2O+
(3)滴定时,将高锰酸钾标准溶液注入酸式滴定管中,滴定到达终点的现象是 .
(4)重复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为 .
Ⅱ.探究过氧化氢的性质
该化学兴趣小组根据所提供的实验条件设计实验证明了过氧化氢的氧化性.(实验条件:试剂只有过氧化氢溶液、氯水、碘化钾淀粉溶液、饱和硫化氢溶液,实验仪器及用品可自选.)
请将他们的实验方法和实验现象填入下表:
Ⅰ.测定过氧化的含量
请填写下列空白:
(1)移取10.00mL密度为ρ g/mL的过氧化氢溶液至250mL容量瓶中,加水稀释至刻度,摇匀.移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样.
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在横线上.
(3)滴定时,将高锰酸钾标准溶液注入酸式滴定管中,滴定到达终点的现象是
(4)重复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为
Ⅱ.探究过氧化氢的性质
该化学兴趣小组根据所提供的实验条件设计实验证明了过氧化氢的氧化性.(实验条件:试剂只有过氧化氢溶液、氯水、碘化钾淀粉溶液、饱和硫化氢溶液,实验仪器及用品可自选.)
请将他们的实验方法和实验现象填入下表:
| 实 验 内 容 | 实 验 方 法 | 实 验 现 象 |
| 验证氧化性 | ||
验证氧化性 |
考点:探究物质的组成或测量物质的含量
专题:实验探究和数据处理题
分析:I.(2)该反应中Mn元素化合价由+7价变为+2价,所以高锰酸根离子作氧化剂,则双氧水作还原剂,所以双氧水中O元素化合价由-1价变为0价,有氧气生成,根据转移电子相等配平方程式;
(3)酸性高锰酸钾完全被还原时,溶液褪色;
(4)根据酸性高锰酸钾和双氧水之间的关系式计算双氧水浓度,双氧水与双氧水溶液的质量之比即为双氧水溶液质量分数;
II.取适量饱和硫化氢溶液于试管中,滴入过氧化氢溶液,产生淡黄色沉淀或溶液变浑浊,证明具有氧化性;验证双氧水的氧化性,也可以加入具有还原性的物质,双氧水能使淀粉碘化钾溶液变蓝色,有明显现象证明.
(3)酸性高锰酸钾完全被还原时,溶液褪色;
(4)根据酸性高锰酸钾和双氧水之间的关系式计算双氧水浓度,双氧水与双氧水溶液的质量之比即为双氧水溶液质量分数;
II.取适量饱和硫化氢溶液于试管中,滴入过氧化氢溶液,产生淡黄色沉淀或溶液变浑浊,证明具有氧化性;验证双氧水的氧化性,也可以加入具有还原性的物质,双氧水能使淀粉碘化钾溶液变蓝色,有明显现象证明.
解答:
解:I.(2)该反应中Mn元素化合价由+7价变为+2价,所以高锰酸根离子作氧化剂,则双氧水作还原剂,所以双氧水中O元素化合价由-1价变为0价,有氧气生成,其转移电子总数为10,所以MnO4-的计量数是2、H2O2,的计量数是5,再结合原子守恒、电荷守恒配平方程式为2MnO4-+5H2O2+6H+=2Mn2++8H2O+502↑,
故答案为:2;5;6;2;8;5;02↑;
(3)酸性高锰酸钾溶液呈酸性,用酸式滴定管量取,该反应中酸性高锰酸钾溶液易被双氧水还原而褪色,但二者恰好完全反应时,再滴入一滴酸性高锰酸钾溶液,溶液呈浅红色且30s内不褪色,
故答案为:滴入一滴高锰酸钾溶液,溶液呈浅红色,且30秒内不褪色;
(4)根据化学方程式5H2O2+6H++2MnO4-=2Mn2++8H2O+502↑,可以得到关系式:2MnO4-~5H2O2,耗用c mol/L KMnO4标准溶液V mL,即cV×10-3mol的高锰酸钾时,所用双氧水的物质的量:2.5cV×10-3mol,则原过氧化氢的质量为:0.025cVmol×34g/mol=0.85cV,过氧化氢溶液中过氧化氢的质量分数为:
=
,
故答案为:
;
Ⅱ.取适量饱和硫化氢溶液于试管中,滴入过氧化氢溶液,产生淡黄色沉淀或溶液变浑浊;如果双氧水能使淀粉碘化钾溶液变蓝色,则说明双氧水氧化碘离子生成碘单质,碘遇淀粉变蓝色,所以能证明双氧水有氧化性;
故答案为:
故答案为:2;5;6;2;8;5;02↑;
(3)酸性高锰酸钾溶液呈酸性,用酸式滴定管量取,该反应中酸性高锰酸钾溶液易被双氧水还原而褪色,但二者恰好完全反应时,再滴入一滴酸性高锰酸钾溶液,溶液呈浅红色且30s内不褪色,
故答案为:滴入一滴高锰酸钾溶液,溶液呈浅红色,且30秒内不褪色;
(4)根据化学方程式5H2O2+6H++2MnO4-=2Mn2++8H2O+502↑,可以得到关系式:2MnO4-~5H2O2,耗用c mol/L KMnO4标准溶液V mL,即cV×10-3mol的高锰酸钾时,所用双氧水的物质的量:2.5cV×10-3mol,则原过氧化氢的质量为:0.025cVmol×34g/mol=0.85cV,过氧化氢溶液中过氧化氢的质量分数为:
| 0.85cV |
| 10.00ml×ρg/ml |
| 17cV |
| 200ρ |
故答案为:
| 17cV |
| 200ρ |
Ⅱ.取适量饱和硫化氢溶液于试管中,滴入过氧化氢溶液,产生淡黄色沉淀或溶液变浑浊;如果双氧水能使淀粉碘化钾溶液变蓝色,则说明双氧水氧化碘离子生成碘单质,碘遇淀粉变蓝色,所以能证明双氧水有氧化性;
| 实 验 内 容 | 实 验 方 法 | 实 验 现 象 |
| 验证氧化性 | 取适量饱和硫化氢溶液于试管中,滴入 过氧化氢溶液. | 产生淡黄色沉淀或溶液变浑浊 |
验证氧化性 | 取适量碘化钾淀粉溶液于试管中,加入过氧化氢溶液 | 溶液变蓝色 |
| 实 验 内 容 | 实 验 方 法 | 实 验 现 象 |
| 验证氧化性 | 取适量饱和硫化氢溶液于试管中,滴入 过氧化氢溶液. | 产生淡黄色沉淀或溶液变浑浊 |
验证氧化性 | 取适量碘化钾淀粉溶液于试管中,加入过氧化氢溶液 | 溶液变蓝色 |
点评:本题考查性质实验方案设计,根据物质性质设计实验进行验证,明确物质的性质是解本题关键,同时考查学生分析问题、实验设计、思维的缜密性等能力,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列除杂方法不正确的是( )
| A、除去乙酸乙酯中混有的少量乙酸:加入饱和碳酸钠溶液,振荡、静置、分液 |
| B、除去乙醇中混有的少量水:加入适量的金属钠,充分反应后蒸馏 |
| C、除去溴苯中混有的少量溴:加入足量的氢氧化钠溶液,振荡、静置、分液 |
| D、除去96%的乙醇中的少量水制无水乙醇:加入生石灰,振荡、静置、蒸馏 |
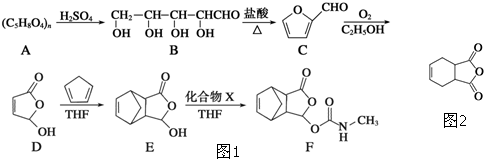
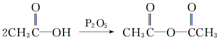 化合物G(结构如图2所示)是合成抗病毒药阿昔洛韦的中间体.请写出以OHCCH(Br)CH2CHO和1,3-丁二烯为原料制备G的合成路线流程图2(无机试剂任用).合成路线流程图示例如下:H2C=CH2
化合物G(结构如图2所示)是合成抗病毒药阿昔洛韦的中间体.请写出以OHCCH(Br)CH2CHO和1,3-丁二烯为原料制备G的合成路线流程图2(无机试剂任用).合成路线流程图示例如下:H2C=CH2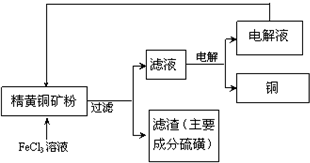 工业上以黄铜矿(主要成分CuFeS2)为原料制备金属铜,有如下两种工艺.
工业上以黄铜矿(主要成分CuFeS2)为原料制备金属铜,有如下两种工艺.
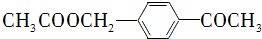 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C═CH2
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C═CH2
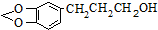 是一种合成药物的中间体,以CH2(COOH)2、CH2Cl2 及
是一种合成药物的中间体,以CH2(COOH)2、CH2Cl2 及 (无机试剂任用)为原料制备该化合物,请将合成该化合物路线流程图补充完整.
(无机试剂任用)为原料制备该化合物,请将合成该化合物路线流程图补充完整.