题目内容
7.根据下列装置组成的原电池填空:
(1)甲中正极发生的反应式为:2H++2e-=H2↑甲中Cu电极现象为:铜片上有气泡生成
(2)乙中负极发生的反应式为:Cu-2e-=Cu2+乙中溶液颜色变化为:溶液变成蓝色.
分析 (1)活泼金属Zn作负极,正极是Cu,正极上电极反应式为2H++2e-=H2↑;
(2)铜更活泼,作负极,失去电子,电极反应式为Cu-2e-=Cu2+,铜离子在溶液中显蓝色.
解答 解:(1)活泼金属Zn作负极,失去电子发生氧化反应,正极是Cu,正极上电极反应式为2H++2e-=H2↑,观察到的现象是铜片上有气泡生成,
故答案为:2H++2e-=H2↑;铜片上有气泡生成;
(2)铜更活泼,作负极,失去电子,电极反应式为Cu-2e-=Cu2+,铜离子在溶液中显蓝色,银作正极,溶液中的银离子在正极得电子产生银单质,
故答案为:Cu-2e-=Cu2+;溶液变成蓝色.
点评 本题考查原电池正负极的判断以及电极反应式的书写,熟悉原电池的工作原理是解题关键,题目比较简单.

练习册系列答案
相关题目
8.有下列物质:①乙烷,②甲醛,③苯酚,④丙烯酸,⑤乙炔.其中与溴水、KMnO4酸性溶液都能反应的是( )
| A. | ①②④ | B. | ②③④⑤ | C. | ①②③ | D. | ②③⑤ |
18.下列物质不是混合物的是( )
| A. | 水玻璃 | B. | 漂白粉 | C. | 冰水 | D. | 氯水 |
2.25℃时,由水电离出c(OH-)=1×10-11mol/L 的溶液中,一定能大量共存的离子组是( )
| A. | Al3+、NH4+、Cl-、SO42- | B. | Na+、CH3COO-、K+、CO32- | ||
| C. | Fe2+、Cl-、Na+、NO3- | D. | K+、NO3-、Cl-、Na+ |
12.下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 常温下,甲基橙呈红色的溶液中:Na+、NH4+、SO42-、CH3COO- | |
| B. | 滴入酚酞试液显红色的溶液:Na+、Ba2+、NO3-、Cl- | |
| C. | 由水电离出的c(H+)=1×10-13mol/L的溶液:NH4+、K+、CO32-、Cl- | |
| D. | 含有大量HCO3-的溶液:K+、Al3+、Cl-、Na+ |
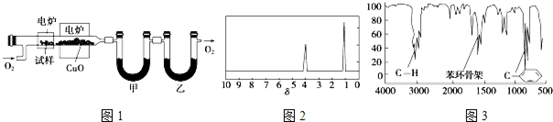
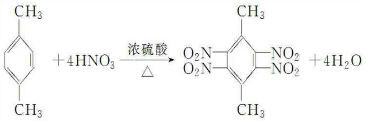 .
.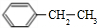 、
、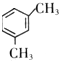 .
.