题目内容
15.关于氧化还原反应,下列说法正确的是( )| A. | 置换反应一定是氧化还原反应 | |
| B. | 氧化还原反应的实质是化合价发生了变化 | |
| C. | 阳离子只有氧化性,阴离子只有还原性 | |
| D. | 氧化还原反应中氧化剂发生了氧化反应 |
分析 A.有元素化合价的升降的反应为氧化还原反应;
B.氧化还原反应的实质是电子的转移,特征是元素化合价的升降;
C.根据离子中某元素的化合价来分析其氧化性或还原性;
D.氧化剂发生了还原反应.
解答 解:A.置换反应有单质参加,一定存在元素化合价的升降,为氧化还原反应,故A正确;
B.氧化还原反应的实质是电子的转移,故B错误;
C.最高价态的阳离子一般具有氧化性,如Fe3+;最低价的阴离子具有还原性,如I-;但Fe2+、SO32-都既有氧化性又有还原性,故C错误;
D.氧化还原反应中氧化剂发生了还原反应,故D错误.
故选A.
点评 本题考查氧化还原反应,为高频考点,侧重于基本概念的理解和应用的考查,注意从元素化合价的角度认识,难度不大.

练习册系列答案
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案
相关题目
19.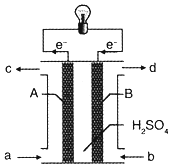 “长征”火箭发射使用的燃料是偏二甲肼(C2H8N2),并使用四氧化二氮作为氧化剂,这种组合的两大优点是,既能在短时间内产生巨大能量将火箭送上太空,产物又不污染空气(产物都是空气成分).某校外研究性学习小组拟将此原理设计为原电池,如图所示,结合学习过的电化学原理分析其设计方案,下列说法正确的是( )
“长征”火箭发射使用的燃料是偏二甲肼(C2H8N2),并使用四氧化二氮作为氧化剂,这种组合的两大优点是,既能在短时间内产生巨大能量将火箭送上太空,产物又不污染空气(产物都是空气成分).某校外研究性学习小组拟将此原理设计为原电池,如图所示,结合学习过的电化学原理分析其设计方案,下列说法正确的是( )
 “长征”火箭发射使用的燃料是偏二甲肼(C2H8N2),并使用四氧化二氮作为氧化剂,这种组合的两大优点是,既能在短时间内产生巨大能量将火箭送上太空,产物又不污染空气(产物都是空气成分).某校外研究性学习小组拟将此原理设计为原电池,如图所示,结合学习过的电化学原理分析其设计方案,下列说法正确的是( )
“长征”火箭发射使用的燃料是偏二甲肼(C2H8N2),并使用四氧化二氮作为氧化剂,这种组合的两大优点是,既能在短时间内产生巨大能量将火箭送上太空,产物又不污染空气(产物都是空气成分).某校外研究性学习小组拟将此原理设计为原电池,如图所示,结合学习过的电化学原理分析其设计方案,下列说法正确的是( )| A. | A为正极 | |
| B. | 电池工作时H+由A极向B极迁移 | |
| C. | 从b 口通入四氧化二氮气体且在B极发生氧化反应 | |
| D. | A极发生的电极反应式:C2H8N2+4H2O+16e-═2CO2+N2+16H+ |
10.下列除杂所选用的试剂或操作方法正确的一组是(括号内为杂质)( )
| 选项 | 待提纯的物质 | 除杂的试剂 | 操作方法 |
| A | CO2(HCl) | 饱和NaHCO3溶液 | 洗气 |
| B | Mg(Al) | HCl | 过滤 |
| C | NaCl(NaHCO3) | HCl | 蒸馏 |
| D | 碘水(I2) | 酒精 | 萃取 |
| A. | A | B. | B | C. | C | D. | D |
20.下列叙述正确的是( )
| A. | 分散质微粒直径的大小关系:溶液>胶体>浊液 | |
| B. | 利用丁达尔效应可以区别溶液与胶体 | |
| C. | 胶体粒子比较小,可以通过半透膜 | |
| D. | 电泳现象可证明胶体属于电解质溶液 |
7.硅及其化合物的应用范围很广.下列说法正确的是( )
| A. | 粗硅制备单晶硅不涉及氧化还原反应 | |
| B. | 硅是人类将太阳能转换为电能的常用材料 | |
| C. | 反应:Si+2NaOH+H2O═Na2SiO3+2H2↑中,Si为还原剂,NaOH和H2O为氧化剂 | |
| D. | 硅能与氢氟酸反应,则硅可以与盐酸反应 |
4.下列关于0.10mol•L-1NaHCO3溶液的说法正确的是( )
| A. | 溶质的电离方程式为:NaHCO3═Na++H++CO32- | |
| B. | 离子浓度关系:c(Na+ )+c(H+ )═c(OH- )+c(HCO3- )+c(CO32-) | |
| C. | 25℃时,加水稀释后,n (H+)与n(OH-)的乘积变大 | |
| D. | 温度升高,c(HCO3-)增大 |