题目内容
9.人们可根据物质的性质,采用适当的方法将混合物中的各物质分离.(1)两种可溶性固体,若它们的溶解度随温度变化而不同,如氯化钠和硝酸钾,可通过降温结晶方法分离.
(2)两种互相溶解但沸点不同的液体,如乙醇与水,可通过蒸馏方法分离.
(3)两种互不相容的液体,如汽油与水,可通过分液方法分离.
分析 (1)溶解度随温度变化而不同,利用结晶法分离;
(2)互溶但沸点不同的液体选择蒸馏法分离;
(3)分层的液体混合物,选择分液法分离.
解答 解:(1)两种可溶性固体,若它们的溶解度随温度变化而不同,如氯化钠和硝酸钾,可通过降温结晶方法分离,故答案为:降温结晶;
(2)两种互相溶解但沸点不同的液体,如乙醇与水,可通过蒸馏方法分离,故答案为:蒸馏;
(3)两种互不相容的液体,如汽油与水,可通过分液方法分离,故答案为:分液.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异、混合物分离方法、实验技能为解答的关键,侧重分析与实验能力的考查,注意分离原理及应用,题目难度不大.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目
15.关于氧化还原反应,下列说法正确的是( )
| A. | 置换反应一定是氧化还原反应 | |
| B. | 氧化还原反应的实质是化合价发生了变化 | |
| C. | 阳离子只有氧化性,阴离子只有还原性 | |
| D. | 氧化还原反应中氧化剂发生了氧化反应 |
16.碱性锌锰电池是日常生活中消耗量最大的电池,其构造如图1所示.放电时总反应为:
Zn+2H2O+2MnO2═Zn(OH)2+2MnOOH
从废旧碱性锌锰电池中回收Zn和MnO2的工艺如图2:
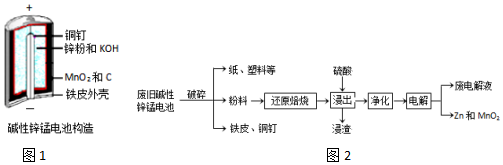
回答下列问题:
(1)MnOOH中,Mn元素的化合价为+3.
(2)“还原焙烧”过程中,高价金属化合物被还原为低价氧化物或金属单质(其中MnOOH、MnO2被还原成MnO),主要原因是“粉料”中含有C.
(3)“净化”是为了除去浸出液中的Fe2+,方法是:加入H2O2(填化学式)溶液将Fe2+氧化为Fe3+,再调节pH使Fe3+完全沉淀.已知浸出液中Mn2+、Zn2+的浓度约为0.1mol•L-1,根据下列数据计算,调节pH的合理范围是3至6.
(离子浓度小于1×10-5mol•L-1即为沉淀完全)
(4)“电解”时,阳极的电极反应式为Mn2+-2e-+2H2O=MnO2+4H+.本工艺中应循环利用的物质是H2SO4(填化学式).
(5)若将“粉料”直接与盐酸共热反应后过滤,滤液的主要成分是ZnCl2和MnCl2.“粉料”中的MnOOH与盐酸反应的化学方程式为2MnOOH+6HCl$\frac{\underline{\;\;△\;\;}}{\;}$2MnCl2+4H2O+Cl2↑.
(6)某碱性锌锰电池维持电流强度0.5A(相当于每秒通过5×10-6 mol电子),连续工作80分钟即接近失效.如果制造一节电池所需的锌粉为6g,则电池失效时仍有87%的金属锌未参加反应.
Zn+2H2O+2MnO2═Zn(OH)2+2MnOOH
从废旧碱性锌锰电池中回收Zn和MnO2的工艺如图2:

回答下列问题:
(1)MnOOH中,Mn元素的化合价为+3.
(2)“还原焙烧”过程中,高价金属化合物被还原为低价氧化物或金属单质(其中MnOOH、MnO2被还原成MnO),主要原因是“粉料”中含有C.
(3)“净化”是为了除去浸出液中的Fe2+,方法是:加入H2O2(填化学式)溶液将Fe2+氧化为Fe3+,再调节pH使Fe3+完全沉淀.已知浸出液中Mn2+、Zn2+的浓度约为0.1mol•L-1,根据下列数据计算,调节pH的合理范围是3至6.
| 化合物 | Mn(OH)2 | Zn(OH)2 | Fe(OH)3 |
| KSP近似值 | 10-13 | 10-17 | 10-38 |
(4)“电解”时,阳极的电极反应式为Mn2+-2e-+2H2O=MnO2+4H+.本工艺中应循环利用的物质是H2SO4(填化学式).
(5)若将“粉料”直接与盐酸共热反应后过滤,滤液的主要成分是ZnCl2和MnCl2.“粉料”中的MnOOH与盐酸反应的化学方程式为2MnOOH+6HCl$\frac{\underline{\;\;△\;\;}}{\;}$2MnCl2+4H2O+Cl2↑.
(6)某碱性锌锰电池维持电流强度0.5A(相当于每秒通过5×10-6 mol电子),连续工作80分钟即接近失效.如果制造一节电池所需的锌粉为6g,则电池失效时仍有87%的金属锌未参加反应.
13.化学用语是学习化学的重要工具,下列化学用语书写正确的是( )
| A. | NH3分子的电子式: | |
| B. | 次氯酸的结构式:H-Cl-O | |
| C. | CH4分子的结构式: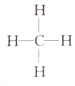 | |
| D. | 用电子式表示氯化氢分子的形成过程: |
4.下列离子方程式正确的是( )
| A. | MgSO4与Ba(OH)2溶液反应:SO42-+Ba2+=Ba SO4↓ | |
| B. | CuSO4溶液吸收H2S气体:Cu2++S2-=CuS↓ | |
| C. | AlCl3 溶液中加入过量的浓氨水:Al3++4NH3•H2O=A1O2-+4NH4++2H2O | |
| D. | 等体积、等浓度的Ba(OH)2稀溶液与NH4HCO3稀溶液混合:Ba2++2OH-+NH4++HCO3-=BaCO3↓+NH3•H2O |
14.已知某有机物A的核磁共振氢谱图如图所示,则该有机物可能是下列中的( )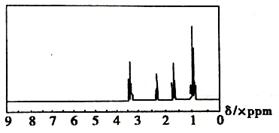

| A. | CH3CH2CH3 | B. | CH3CH2CH2OH | C. | CH3CH2CH2CH3 | D. | CH3CH2CHO |
18.化学与人类生产、生活、社会可持续发展密切相关,下列说法错误的是( )
| A. | 为防止中秋月饼等富脂食品氧化变质,常在包装袋中放入硅胶 | |
| B. | “天宫一号”中使用的碳纤维,是一种新型无机非金属材料 | |
| C. | 二氧化硅可用于光纤通信、单晶硅可用于光电转换 | |
| D. | 淀粉、油脂和蛋白质都是高分子化合物 |
19.向二氯化铂的HCl溶液中通入乙烯气体,再加入KCl可得K[Pt(C2H4)Cl3]•H2O (蔡氏盐),下列有关化学用语表示正确的是( )
| A. | KCl的电子式: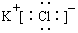 | |
| B. | 乙烯的结构简式:CH2CH2 | |
| C. | 中子数为117,质子数为78 的铂原子:${\;}_{117}^{195}Pt$ | |
| D. | K+的结构示意图: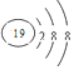 |