题目内容
4.下列关于0.10mol•L-1NaHCO3溶液的说法正确的是( )| A. | 溶质的电离方程式为:NaHCO3═Na++H++CO32- | |
| B. | 离子浓度关系:c(Na+ )+c(H+ )═c(OH- )+c(HCO3- )+c(CO32-) | |
| C. | 25℃时,加水稀释后,n (H+)与n(OH-)的乘积变大 | |
| D. | 温度升高,c(HCO3-)增大 |
分析 A.NaHCO3为强电解质,弱酸的酸式酸根离子不能拆分;
B.溶液遵循电荷守恒;
C.加水促进水解,生成n(OH-)增大,Kw不变;
D.盐类水解为吸热反应,升高温度,水解平衡正向移动.
解答 解:A.溶质的电离方程式为NaHCO3═Na++HCO3-,故A错误;
B.离子浓度关系为c(Na+)+c(H+)═c(OH- )+c(HCO3- )+2c(CO32-),遵循电荷守恒,故B错误;
C.加水促进水解,生成n(OH-)增大,Kw不变,c(OH- )减小,则c(H+ )增大,n (H+)与n(OH-)的乘积变大,故C正确;
D.升高温度,水解平衡正向移动,则c(HCO3-)减小,故D错误;
故选C.
点评 本题考查离子浓度大小的比较,为高频考点,把握电荷守恒、盐类水解为解答的关键,侧重分析与应用能力的考查,注意选项C为解答的易错点,题目难度不大.

练习册系列答案
 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案
相关题目
14.下列解释事实的化学(或离子)方程式正确的是( )
| A. | 盛放NaOH溶液的试剂瓶不能用玻璃塞:SiO2+2OH-═SiO32-+H2O | |
| B. | 用食醋检验牙膏中的摩擦剂碳酸钙:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| C. | 用氯化铁溶液腐蚀铜线路板:Cu+Fe3+═Fe2++Cu2+ | |
| D. | 用氢氧化钠溶液去除铝表面的氧化膜:Al2O3+2OH-═2AlO2-+H2↑ |
15.关于氧化还原反应,下列说法正确的是( )
| A. | 置换反应一定是氧化还原反应 | |
| B. | 氧化还原反应的实质是化合价发生了变化 | |
| C. | 阳离子只有氧化性,阴离子只有还原性 | |
| D. | 氧化还原反应中氧化剂发生了氧化反应 |
12.NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 8g CH4O中含有的C-H键数目为NA | |
| B. | 25℃时,100mL pH=8的氨水中NH4+的个数为9.9×10-8NA | |
| C. | 56g Fe和64g Cu分别与1 mol S反应转移的电子数均为2NA | |
| D. | 标准状况下,2.24 LCl2溶于水所得氯水中含氯的微粒总数为0.2NA |
19.在给定的条件下,下列选项所示的物质间转化均能一步实现的是( )
| A. | SiO2$→_{△}^{NaOH(aq)}$Na2SiO3$\stackrel{CO_{2}}{→}$H2SiO3 | |
| B. | S$→_{点燃}^{O_{2}}$SO2$\stackrel{BaCl_{2}(aq)}{→}$BaSO3 | |
| C. | NH3$→_{催化剂/△}^{O_{2}}$NO2$\stackrel{H_{2}O}{→}$HNO3 | |
| D. | MgCl2•6H2O$\stackrel{△}{→}$MgCl2$\stackrel{电解}{→}$Mg |
9.化学与生产、生活、社会密切相关.下列说法正确的是( )
| A. | 硅胶可用作食品干燥剂和催化剂的载体 | |
| B. | 铝盐、铁盐净水原理与氯气净水原理相同 | |
| C. | 浸泡过高锰酸钾溶液的硅藻土放于新鲜的水果箱内是为了催熟水果 | |
| D. | 电解熔融NaC1或A1C13制取Na或A1 |
16.碱性锌锰电池是日常生活中消耗量最大的电池,其构造如图1所示.放电时总反应为:
Zn+2H2O+2MnO2═Zn(OH)2+2MnOOH
从废旧碱性锌锰电池中回收Zn和MnO2的工艺如图2:
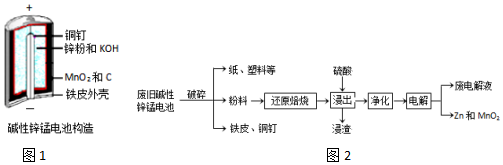
回答下列问题:
(1)MnOOH中,Mn元素的化合价为+3.
(2)“还原焙烧”过程中,高价金属化合物被还原为低价氧化物或金属单质(其中MnOOH、MnO2被还原成MnO),主要原因是“粉料”中含有C.
(3)“净化”是为了除去浸出液中的Fe2+,方法是:加入H2O2(填化学式)溶液将Fe2+氧化为Fe3+,再调节pH使Fe3+完全沉淀.已知浸出液中Mn2+、Zn2+的浓度约为0.1mol•L-1,根据下列数据计算,调节pH的合理范围是3至6.
(离子浓度小于1×10-5mol•L-1即为沉淀完全)
(4)“电解”时,阳极的电极反应式为Mn2+-2e-+2H2O=MnO2+4H+.本工艺中应循环利用的物质是H2SO4(填化学式).
(5)若将“粉料”直接与盐酸共热反应后过滤,滤液的主要成分是ZnCl2和MnCl2.“粉料”中的MnOOH与盐酸反应的化学方程式为2MnOOH+6HCl$\frac{\underline{\;\;△\;\;}}{\;}$2MnCl2+4H2O+Cl2↑.
(6)某碱性锌锰电池维持电流强度0.5A(相当于每秒通过5×10-6 mol电子),连续工作80分钟即接近失效.如果制造一节电池所需的锌粉为6g,则电池失效时仍有87%的金属锌未参加反应.
Zn+2H2O+2MnO2═Zn(OH)2+2MnOOH
从废旧碱性锌锰电池中回收Zn和MnO2的工艺如图2:

回答下列问题:
(1)MnOOH中,Mn元素的化合价为+3.
(2)“还原焙烧”过程中,高价金属化合物被还原为低价氧化物或金属单质(其中MnOOH、MnO2被还原成MnO),主要原因是“粉料”中含有C.
(3)“净化”是为了除去浸出液中的Fe2+,方法是:加入H2O2(填化学式)溶液将Fe2+氧化为Fe3+,再调节pH使Fe3+完全沉淀.已知浸出液中Mn2+、Zn2+的浓度约为0.1mol•L-1,根据下列数据计算,调节pH的合理范围是3至6.
| 化合物 | Mn(OH)2 | Zn(OH)2 | Fe(OH)3 |
| KSP近似值 | 10-13 | 10-17 | 10-38 |
(4)“电解”时,阳极的电极反应式为Mn2+-2e-+2H2O=MnO2+4H+.本工艺中应循环利用的物质是H2SO4(填化学式).
(5)若将“粉料”直接与盐酸共热反应后过滤,滤液的主要成分是ZnCl2和MnCl2.“粉料”中的MnOOH与盐酸反应的化学方程式为2MnOOH+6HCl$\frac{\underline{\;\;△\;\;}}{\;}$2MnCl2+4H2O+Cl2↑.
(6)某碱性锌锰电池维持电流强度0.5A(相当于每秒通过5×10-6 mol电子),连续工作80分钟即接近失效.如果制造一节电池所需的锌粉为6g,则电池失效时仍有87%的金属锌未参加反应.
13.化学用语是学习化学的重要工具,下列化学用语书写正确的是( )
| A. | NH3分子的电子式: | |
| B. | 次氯酸的结构式:H-Cl-O | |
| C. | CH4分子的结构式: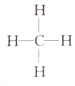 | |
| D. | 用电子式表示氯化氢分子的形成过程: |
18.化学与人类生产、生活、社会可持续发展密切相关,下列说法错误的是( )
| A. | 为防止中秋月饼等富脂食品氧化变质,常在包装袋中放入硅胶 | |
| B. | “天宫一号”中使用的碳纤维,是一种新型无机非金属材料 | |
| C. | 二氧化硅可用于光纤通信、单晶硅可用于光电转换 | |
| D. | 淀粉、油脂和蛋白质都是高分子化合物 |