题目内容
19.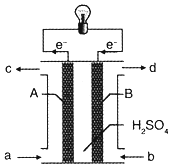 “长征”火箭发射使用的燃料是偏二甲肼(C2H8N2),并使用四氧化二氮作为氧化剂,这种组合的两大优点是,既能在短时间内产生巨大能量将火箭送上太空,产物又不污染空气(产物都是空气成分).某校外研究性学习小组拟将此原理设计为原电池,如图所示,结合学习过的电化学原理分析其设计方案,下列说法正确的是( )
“长征”火箭发射使用的燃料是偏二甲肼(C2H8N2),并使用四氧化二氮作为氧化剂,这种组合的两大优点是,既能在短时间内产生巨大能量将火箭送上太空,产物又不污染空气(产物都是空气成分).某校外研究性学习小组拟将此原理设计为原电池,如图所示,结合学习过的电化学原理分析其设计方案,下列说法正确的是( )| A. | A为正极 | |
| B. | 电池工作时H+由A极向B极迁移 | |
| C. | 从b 口通入四氧化二氮气体且在B极发生氧化反应 | |
| D. | A极发生的电极反应式:C2H8N2+4H2O+16e-═2CO2+N2+16H+ |
分析 由电子转移方向可知A为负极,偏二甲肼被氧化石花菜氮气和二氧化碳,电极方程式为C2H8N2-16e-+4H2O=2CO2+N2+16H+,B为正极,发生还原反应,四氧化二氮被还原生成氮气,电极方程式为N2O4+8e-+8H+=N2+4H2O,结合电极方程式解答该题.
解答 解:A.由电子转移方向可知A为负极,B为正极,故A错误;
B.原电池工作时H+由负极向正极移动,即A极向B极迁移,故B正确;
C.A为负极,则从a口通入偏二甲肼,从b 口通入四氧化二氮气体且在B极发生还原反应,故C错误;
D.偏二甲肼被氧化为氮气和二氧化碳,电极方程式为C2H8N2-16e-+4H2O=2CO2+N2+16H+,故D错误.
故选B.
点评 本题考查化学电源新型电池,为高频考点,侧重于学生的分析能力的考查,本题难度不大,注意电极反应式的书写,以此判断各电极的变化.

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目
9.下列离子方程式的书写正确的是( )
| A. | 大理石溶于醋酸中:CaCO3+2CH3COOH═Ca2++2CH3COO-+CO2↑+H2O | |
| B. | H2SO4溶液与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| C. | 将Na投入到CuSO4溶液中:2Na+Cu2+═2Na++Cu↓ | |
| D. | 将Cl2通入水中:Cl2+H2O═2H-+Cl-+ClO- |
10.下列与化学有关的说法中正确的是( )
| A. | 在0.1mol/lHNO3溶液中加入FeCO3粉末,发生反应的离子方程式为:2FeCO3+2H+═2Fe2++CO2↑+H2O | |
| B. | 在$\frac{c(O{H}^{-})}{c({H}^{+})}$=1010的溶液中NO3-、I-、Na+、SO42-不能大量共存 | |
| C. | 25℃时pH=13的NaOH溶液中含有OH-的数目为0.1 NA | |
| D. | 闭容器中2molNO与1molO2充分反应,产物的分子数小于2NA |
14.向四支试管中分别加入少量不同的无色溶液进行如下操作,结论正确的是( )
| 操 作 | 现 象 | 结 论 | |
| A | 滴加稀NaOH溶液,将红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH4+ |
| B | 向溶液X 中先滴加稀硝酸,再滴加Ba(NO3)2溶液 | 出现白色沉淀 | 溶液X 中一定含有SO42- |
| C | 滴加氯水和CCl4,振荡、静置 | 下层溶液显紫色 | 原溶液中有I- |
| D | 用洁净铂丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中有Na+、无K+ |
| A. | A | B. | B | C. | C | D. | D |
4.下列装置用于实验室制备氨气并配制银氨溶液,不能达到实验目的是( )
| A. | 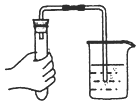 检查气密性 检查气密性 | B. |  制备氨气 | C. | 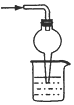 吸收氨尾气 | D. | 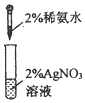 配制银氨溶液 |
11.常温下,下列溶液中微粒的物质的量浓度关系正确的是( )
| A. | 将浓度均为0.10mol•L-1的CH3COONH4与CH3COONa溶液等体积混合:c(CH3COO-)>c(Na+)>c(NH4+)>c(OH-) | |
| B. | 向0.10mol•L-1CH3COONa溶液中滴加盐酸至溶液呈中性:c(Cl-)>c(Na+)>c(H+)=c(OH-) | |
| C. | 将0.10mol•L-1KHC2O4和0.10mol•L-1K2C2O4溶液等体积混合所得溶液中:2c(K+)=3c(C2O42-)+3c(HCO4) | |
| D. | 将等物质的量浓度的NH4HCO3与NaCl溶液等体积混合,析出部分NaHCO3晶体后的溶液(pH<7)中:c(H+)+c(H2CO3)=c(OH-)+c(CO32-)+c(NH3•H2O) |
14.下列解释事实的化学(或离子)方程式正确的是( )
| A. | 盛放NaOH溶液的试剂瓶不能用玻璃塞:SiO2+2OH-═SiO32-+H2O | |
| B. | 用食醋检验牙膏中的摩擦剂碳酸钙:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| C. | 用氯化铁溶液腐蚀铜线路板:Cu+Fe3+═Fe2++Cu2+ | |
| D. | 用氢氧化钠溶液去除铝表面的氧化膜:Al2O3+2OH-═2AlO2-+H2↑ |
15.关于氧化还原反应,下列说法正确的是( )
| A. | 置换反应一定是氧化还原反应 | |
| B. | 氧化还原反应的实质是化合价发生了变化 | |
| C. | 阳离子只有氧化性,阴离子只有还原性 | |
| D. | 氧化还原反应中氧化剂发生了氧化反应 |

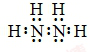 ;N2H4在水中的第一步电离方程式为N2H4+H2O?N2H5++OH-
;N2H4在水中的第一步电离方程式为N2H4+H2O?N2H5++OH-