题目内容
常温下,pH相等的氨水和氢氧化钠溶液中的c(NH4+)和c(Na+)比较,则( )
| A、相等 | B、前者大 |
| C、后者大 | D、无法比较 |
考点:弱电解质在水溶液中的电离平衡,溶液pH的定义
专题:电离平衡与溶液的pH专题
分析:常温下,pH相等的氨水和NaOH溶液中c(OH-)相等,根据电荷守恒判断c(NH4+)、c(Na+)的相对大小,据此分析解答.
解答:
解:常温下,pH相等的氨水和NaOH溶液中c(OH-)相等,溶液中存在电荷守恒,根据电荷守恒得c(OH-)=c(NH4+)+c(H+)=c(Na+)+c(H+),相同温度下水的离子积常数相等,氢氧根离子浓度相等,则溶液中氢离子浓度相等,所以c(NH4+)=c(Na+),故选A.
点评:本题考查了离子浓度大小比较,根据溶液的pH再结合电荷守恒、离子积常数进行计算即可,题目难度不大.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
 如图是198K时N2与H2反应过程中能量变化曲线.下列叙述正确的是( )
如图是198K时N2与H2反应过程中能量变化曲线.下列叙述正确的是( )| A、该反应的热化学方程式为N2+3H2?2NH3△H=-92 kJ?mol-1 |
| B、b曲线是加入催化剂时的能量变化曲线 |
| C、加入催化剂,该化学反应的反应热发生改变 |
| D、温度、体积一定,1 mol N2和3 mol H2反应后放出的热量为Q1 kJ,若2 mol N2和6 mol H2反应后放出的热量为Q2 kJ,则184>Q2>2Q1 |
为了检验某氯代烃中的氯元素,现进行如下操作.其中合理的是( )
| A、取氯代烃少许,加入AgNO3溶液 |
| B、取氯代烃少许与NaOH水溶液共热,然后加入AgNO3溶液 |
| C、取氯代烃少许与NaOH水溶液共热后,加入稀硝酸酸化,再加入AgNO3溶液 |
| D、取氯代烃少许与NaOH乙醇溶液共热后,再加入AgNO3溶液 |
二甘醇可用作溶剂、纺织助剂等,一旦进入人体会导致急性肾衰竭,危及生命.二甘醇的结构简式是HO-CH2CH2-O-CH2CH2-OH.下列有关二甘醇的叙述正确的是( )
| A、不能发生消去反应 |
| B、能发生取代反应也能发生氧化反应 |
| C、能溶于水,不溶于乙醇 |
| D、符合通式CnH2nO3 |
下列各溶液中,pH最大的是( )
| A、pH=5的盐酸溶液稀释1000倍 |
| B、pH=9的烧碱溶液稀释1000倍 |
| C、pH=9的氨水稀释1000倍 |
| D、pH=4的盐酸溶液与pH=10的烧碱溶液等体积混合 |
下列化学用语正确的是( )
A、氮气的电子式: |
B、氯原子的结构示意图: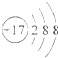 |
C、水分子的结构式: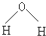 |
D、CH4分子的球棍模型: |
下列叙述正确的是( )
| A、同温同压下,相同体积的物质,它们的物质的量必相等 |
| B、等体积、等物质的量浓度的强酸中所含的H+数目一定相等 |
| C、1 L一氧化碳气体的质量一定比1 L氧气的质量小 |
| D、任何条件下,等物质的量的乙烯和一氧化碳所含的分子数必相等 |
下列叙述不正确的是( )
| A、使用无磷洗衣粉是降低水体富营养化的方法之一 |
| B、海啸使水源发生污染用明矾进行净化和消毒 |
| C、SO2和NO2都能使雨水的pH<5.6造成酸雨 |
| D、合理开发和利用可燃冰(固态甲烷水合物)有助于缓解能源紧缺 |