题目内容
下列化学用语正确的是( )
A、氮气的电子式: |
B、氯原子的结构示意图: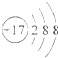 |
C、水分子的结构式: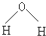 |
D、CH4分子的球棍模型: |
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.氮气的电子式中漏掉了氮原子的1对孤电子对;
B.氮原子的核电荷数和最外层电子数都是17,最外层电子数为7;
C.水分子中存在两个氧氢键,为V型结构;
D.根据甲烷的球棍模型和比例模型的表示方法进行判断.
B.氮原子的核电荷数和最外层电子数都是17,最外层电子数为7;
C.水分子中存在两个氧氢键,为V型结构;
D.根据甲烷的球棍模型和比例模型的表示方法进行判断.
解答:
解:A.氮气分子中存在氮氮三键,氮原子最外层为8电子,氮气正确的电子式为: ,故A错误;
,故A错误;
B.氯原子不带电荷,最外层为7个电子,氯原子的结构示意图为: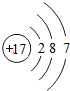 ,故B错误;
,故B错误;
C.水分子中存在两个氧氢键,为V型结构,水的结构式为: ,故C正确;
,故C正确;
D.甲烷中存在4个碳氢键,甲烷为正四面体结构, 为甲烷的球棍模型,甲烷的球棍模型为:
为甲烷的球棍模型,甲烷的球棍模型为: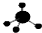 ,故D错误;
,故D错误;
故选C.
 ,故A错误;
,故A错误;B.氯原子不带电荷,最外层为7个电子,氯原子的结构示意图为:
 ,故B错误;
,故B错误;C.水分子中存在两个氧氢键,为V型结构,水的结构式为:
 ,故C正确;
,故C正确;D.甲烷中存在4个碳氢键,甲烷为正四面体结构,
 为甲烷的球棍模型,甲烷的球棍模型为:
为甲烷的球棍模型,甲烷的球棍模型为: ,故D错误;
,故D错误;故选C.
点评:本题考查了电子式、结构式、原子结构示意图、球棍模型与比例模型的判断,题目难度中等,注意掌握常见化学用语的概念及正确的表示方法,明确球棍模型与比例模型的区别.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
下列说法不正确的是( )
| A、1mol氧气中含有12.04×1023个氧原子,在标准状况下占有体积22.4L |
| B、500mL1.0 mol?L-1NaNO2溶液含有溶质质量为34.5g |
| C、等体积、浓度均为1mol/L的磷酸和盐酸,电离出的氢离子数之比小于3:1 |
| D、1.00molNaCl中含有6.02×1023个NaCl分子,欲配制1.00L,1.00mol.L-1的NaCl溶液,可将 58.5gNaCl溶于 1.00L水中 |
与元素的化学性质关系最密切的是( )
| A、核外电子总数 |
| B、核内质子数 |
| C、最外层电子数 |
| D、相对原子质量 |
将甲和乙组成的混合气体通入丙溶液,一定能产生沉淀的是( )
| 甲 | 乙 | 丙 | |
| A | NO2 | SO2 | BaCl2 |
| B | HCl | CO2 | 石灰水 |
| C | CO2 | SO2 | 石灰水 |
| D | CO2 | NH3 | CaCl2 |
| A、A | B、B | C、C | D、D |
常温下,pH相等的氨水和氢氧化钠溶液中的c(NH4+)和c(Na+)比较,则( )
| A、相等 | B、前者大 |
| C、后者大 | D、无法比较 |
在相同条件下完全燃烧甲烷、丙烷、乙烯.如使产生的水蒸气(相同状况)的体积相等,则所需三种气体的质量比是( )
| A、8:?11:?14 |
| B、4:?22:?7 |
| C、1:?2:?1 |
| D、2:?1:?2 |
以下是几种常用基本物理量的名称与符号的对应关系,其中不正确的是( )
| A、物质的量mol |
| B、质量m |
| C、时间t |
| D、物质的量浓度C |
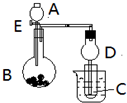 用如图所示装置进行实验,将A逐滴加入B中:
用如图所示装置进行实验,将A逐滴加入B中: