题目内容
最近医学界通过用放射性14C标记C60的羧酸衍生物在特定条件下可通过断裂DNA杀死细胞,从而抑制艾滋病(AIDS),下列有关14C的叙述正确的是( )
| A、与普通碳原子的化学性质不同 |
| B、与14N含的中子数相同 |
| C、是金刚石的同素异形体 |
| D、与12C互为同位素 |
考点:同位素及其应用,核素
专题:原子组成与结构专题
分析:A.碳原子的化学性质相同;
B.中子数=质量数-质子数;
C.同素异形体为同种元素的不同单质;
D.质子数相同,中子数不同的原子互为同位素.
B.中子数=质量数-质子数;
C.同素异形体为同种元素的不同单质;
D.质子数相同,中子数不同的原子互为同位素.
解答:
解:A.15C与C60中普通碳原子,为同种元素的碳原子,则碳原子的化学性质相同,故A错误;
B.15C的中子数为15-6=9,14N的中子为14-7=7,二者不同,故B错误;
C.金刚石为单质,但14C为原子,二者不是同素异形体,故C错误;
D.15C与12C的质子数均为6,中子数不同,互为同位素,故D正确;
故选D.
B.15C的中子数为15-6=9,14N的中子为14-7=7,二者不同,故B错误;
C.金刚石为单质,但14C为原子,二者不是同素异形体,故C错误;
D.15C与12C的质子数均为6,中子数不同,互为同位素,故D正确;
故选D.
点评:本题考查原子的构成及原子中的数量关系,明确质量数、质子数、中子数的关系及同位素、同素异形体即可解答,较简单.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
人体正常的血红蛋白中含有Fe2+,若误食亚硝酸盐,则使血红蛋白中Fe2+转化为Fe3+丧失其生理功能,临床证明服用维生素C可以解毒.下列叙述正确的是( )
| A、中毒反应中亚硝酸盐是氧化剂 |
| B、中毒反应中Fe3+是氧化剂 |
| C、维生素C能将亚硝酸盐氧化成硝酸盐,使其解毒 |
| D、维生素C能将Fe3+还原为Fe2+,使其解毒 |
下列说法正确的是( )
| A、32克氧气占有的体积约为22.4L |
| B、22.4L氮气含有阿佛加德罗常数个氮气分子 |
| C、在标况下22.4L水的质量约为18克 |
| D、22克二氧化碳与标况下11.2 LHCl约含有相同的分子数 |
2012年2月,国务院同意发布新修订的《环境空气质量标准》增加了PM2.5监测指标,PM2.5是用来监测空气中下列哪项含量的( )
| A、二氧化碳 | B、一氧化碳 |
| C、二氧化硫 | D、可吸入颗粒物 |
某水溶液中含有等物质的量的Cu2+、Cl-、H+、SO42-,该溶液放在电解槽中,下列说法正确的是( )
| A、用石墨做电极时,首先在阴极放电的是Cl- |
| B、用石墨做电极时,电解一段时间后H+有可能在阴极放电 |
| C、用铁做电极时,阳极反应式:2Cl--2e-=Cl2↑ |
| D、用石墨做电极时,开始电解时Cl-与H+首先放电 |
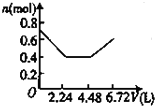
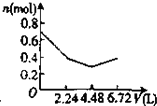
2mol A与2mol B混合于2L的密闭容器中,发生如下反应:2A(g)+3B(g)?2C(g)+zD(g),若2s后,A的转化率为50%,测得v(D)=0.25mol?L-1?s-1,下列推断正确的是( )
| A、v(B)=0.75 mol?L-1?s-1 |
| B、z=2 |
| C、B的转化率为25% |
| D、C的体积分数约为28.6% |


 保险粉(Na2S2O4)有极强的还原性,遇水或在潮湿空气中会分解发热,甚至引起燃烧,但在碱性环境下较稳定.某实验小组利用如图装置制取保险粉,并验证其还原性.在35~45℃下,将SO2气体通入锌粉-水悬浮液中,生成ZnS2O4;待反应完全后,冷却至室温,向三颈烧瓶中加入18%的NaOH溶液,生成Na2S2O4和Zn(OH)2;经一系列操作获得无水Na2S2O4样品.
保险粉(Na2S2O4)有极强的还原性,遇水或在潮湿空气中会分解发热,甚至引起燃烧,但在碱性环境下较稳定.某实验小组利用如图装置制取保险粉,并验证其还原性.在35~45℃下,将SO2气体通入锌粉-水悬浮液中,生成ZnS2O4;待反应完全后,冷却至室温,向三颈烧瓶中加入18%的NaOH溶液,生成Na2S2O4和Zn(OH)2;经一系列操作获得无水Na2S2O4样品.