题目内容
下列说法正确的是( )
| A、32克氧气占有的体积约为22.4L |
| B、22.4L氮气含有阿佛加德罗常数个氮气分子 |
| C、在标况下22.4L水的质量约为18克 |
| D、22克二氧化碳与标况下11.2 LHCl约含有相同的分子数 |
考点:阿伏加德罗定律及推论
专题:计算题,阿伏加德罗常数和阿伏加德罗定律
分析:根据n=
=
=
计算,注意气体存在的条件,以此解答.
| m |
| M |
| V |
| Vm |
| N |
| NA |
解答:
解:A.气体存在的条件未知,不能确定体积,故A错误;
B.气体存在的条件未知,不能确定物质的量,故B错误;
C.在标况下水为液体,不能根据气体的摩尔体积计算,故C错误;
D.二氧化碳的物质的量为
=0.5mol,11.2 LHCl的物质的量为
=0.5mol,物质的量相等,则分子数相等,故D正确.
故选D.
B.气体存在的条件未知,不能确定物质的量,故B错误;
C.在标况下水为液体,不能根据气体的摩尔体积计算,故C错误;
D.二氧化碳的物质的量为
| 22g |
| 44g/mol |
| 11.2L |
| 22.4L/mol |
故选D.
点评:本题考查阿伏伽德罗定律及其推论,为高频考点,侧重于学生的分析能力的考查,注意把握相关计算公式的运用以及阿伏伽德罗定律的理解,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
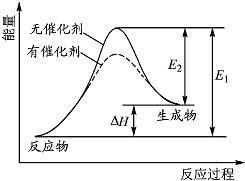 2HI(g)?H2(g)+I2(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
2HI(g)?H2(g)+I2(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )| A、升高温度,反应速率增大,△H减小 |
| B、升高温度,不影响活化分子百分数 |
| C、催化剂能降低该反应的活化能 |
| D、逆反应的活化能等于正反应的活化能 |
如图是某同学从化学试剂商店买回的硫酸试剂标签上的部分内容.下列说法正确的( ) 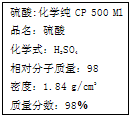

| A、该硫酸的物质的量浓度为9.2 mol/L |
| B、12gC与足量该硫酸共热反应,生成标准状况下气体体积为44.8L |
| C、1 mol Fe与足量的该硫酸反应产生2 g氢气 |
| D、配制200 mL 4.6 mol/L的稀硫酸需取该硫酸50 mL |
下列离子方程式中,正确的是( )
| A、铜片插入硝酸银溶液中:Cu+Ag+═Cu2++Ag |
| B、大理石溶于醋酸的反应:CaCO3+2CH3COOH═Ca2++2CH3COO-+CO2↑+H2O |
| C、向稀硫酸溶液中加入铁粉:2Fe+6H+═2Fe3++3H2↑ |
| D、稀硫酸跟氢氧化钡溶液混合:H++OH-═H2O |
下列两种气体的分子数一定相等的是( )
| A、质量相等、密度不等的氮气和二氧化碳 |
| B、等体积、等密度的一氧化碳和氮气 |
| C、等温、等体积的氧气和氮气 |
| D、等压强、等体积的氮气和二氧化碳 |
下列对溶液、胶体和浊液的认识正确的是( )
| A、三种分散系的分散质均能通过滤纸 |
| B、胶体在一定的条件下也能稳定存在 |
| C、溶液和胶体通常都是无色透明的液体,而浊液不透明 |
| D、胶体区别于其他分散系的本质特征是产生丁达尔现象 |
最近医学界通过用放射性14C标记C60的羧酸衍生物在特定条件下可通过断裂DNA杀死细胞,从而抑制艾滋病(AIDS),下列有关14C的叙述正确的是( )
| A、与普通碳原子的化学性质不同 |
| B、与14N含的中子数相同 |
| C、是金刚石的同素异形体 |
| D、与12C互为同位素 |