题目内容
下列各组中的两个反应,可用同一离子方程式表示的是( )
| A、CaCO3和HCl、Na2CO3和HCl |
| B、BaCl2和H2SO4、Ba(OH)2和H2SO4 |
| C、HNO3和K2CO3、HCl和NaHCO3 |
| D、KOH和H2SO4、Ba(OH)2和HNO3 |
考点:离子方程式的书写
专题:离子反应专题
分析:A.碳酸钙在离子反应中保留化学式;
B.硫酸钡、水在离子反应中均保留化学式;
C.碳酸根离子、碳酸氢根离子在离子反应中不能拆分;
D.反应均生成可溶性盐和水.
B.硫酸钡、水在离子反应中均保留化学式;
C.碳酸根离子、碳酸氢根离子在离子反应中不能拆分;
D.反应均生成可溶性盐和水.
解答:
解:A.CaCO3和HCl、Na2CO3和HCl的离子反应分别为CaCO3+2H+=Ca2++CO2↑+H2O、CO32-+2H+=CO2↑+H2O,故A不选;
B.BaCl2和H2SO4、Ba(OH)2和H2SO4离子反应分别为SO42-+Ba2+=BaSO4↓、2OH-+2H++SO42-+Ba2+=BaSO4↓+2H2O,故B不选;
C.HNO3和K2CO3、HCl和NaHCO3的离子反应为CO32-+2H+=CO2↑+H2O、HCO3-+H+=CO2↑+H2O,故C不选;
D.KOH和H2SO4、Ba(OH)2和HNO3的离子反应均为OH-+H+=H2O,故D选;
故选D.
B.BaCl2和H2SO4、Ba(OH)2和H2SO4离子反应分别为SO42-+Ba2+=BaSO4↓、2OH-+2H++SO42-+Ba2+=BaSO4↓+2H2O,故B不选;
C.HNO3和K2CO3、HCl和NaHCO3的离子反应为CO32-+2H+=CO2↑+H2O、HCO3-+H+=CO2↑+H2O,故C不选;
D.KOH和H2SO4、Ba(OH)2和HNO3的离子反应均为OH-+H+=H2O,故D选;
故选D.
点评:本题考查离子反应方程式的书写,为高频考点,把握发生的化学反应及离子反应的书写方法为解答的关键,侧重复分解反应的离子反应考查,注意离子反应中保留化学式的物质,题目难度不大.

练习册系列答案
相关题目
下列离子方程式中正确的是( )
| A、铜片上滴稀硫酸:Cu+2H+=Cu2++H2↑ | ||||
B、MnO2与浓盐酸反应制Cl2:MnO2+4HCl
| ||||
| C、少量二氧化硫与烧碱溶液反应:SO2+2OHˉ=SO32ˉ+H2O | ||||
| D、氯气和冷的氢氧化钠溶液反应:2Cl2+2OHˉ=3Clˉ+ClOˉ+H2O |
下列说法中正确的是( )
| A、树状分类法是唯一能表示物质分类的方法 |
| B、等浓度、等体积的磷酸和盐酸,电离出的氢离子数之比为3:1 |
| C、向氢氧化铁胶体中滴加稀硫酸,开始时产生沉淀,继续滴加时沉淀溶解 |
| D、胶体、溶液、浊液分属不同类别的本质是其透过滤纸的性质不同 |
下列说法正确的是( )
| A、原电池中电子流入的一极是正极,发生氧化反应 |
| B、2A(g)?B(g)+3C(g)△H<0 反应物总能量低于生成总能量 |
| C、在101kPa时,1molH2完全燃烧生成水蒸气所放出的热量为氢气的燃烧热 |
| D、原电池工作时,电解质溶液中阴离子移向负极 |
下列反应的离子方程式书写正确的是( )
| A、AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ |
| B、氢氧化钡溶液与稀 H2SO4:Ba2++OH-+SO42-+H+═BaSO4↓+H2O |
| C、向氯化亚铁溶液中通入氯气:2Fe2++Cl2═2Fe3++2Cl- |
| D、过量氯气通入溴化亚铁溶液中2Fe2++2Br-+2Cl2═Fe3++Br2+4Cl- |
HA为酸性略强于醋酸的一元弱酸.在0.1mol?L-1 NaA溶液中,离子浓度关系正确的是( )
| A、c(Na+)>c(A-)>c(H+)>c(OH-) |
| B、c(Na+)>c(OH-)>c(A-)>c(H+) |
| C、c(Na+)+c(OH-)=c(A-)+c(H+) |
| D、c(Na+)+c(H+)=c(A-)+c(OH-) |
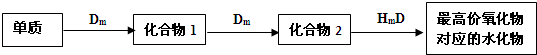
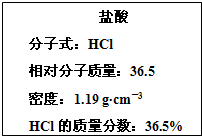 如图为实验室某浓盐酸试剂瓶上的标签的有关内容,试根据标签上的有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶上的标签的有关内容,试根据标签上的有关数据回答下列问题: