题目内容
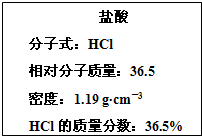 如图为实验室某浓盐酸试剂瓶上的标签的有关内容,试根据标签上的有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶上的标签的有关内容,试根据标签上的有关数据回答下列问题:(1)该浓盐酸中HCl的物质的量浓度为
(2)取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D.溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制500mL物质的量浓度为0.400mol/L的稀盐酸.
①该学生需要量取
②配制该溶液所需玻璃仪器除烧杯、玻璃棒、胶头滴管外,还需要
③在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在短线上填“偏高”、“偏低”或“无影响”).
Ⅰ.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水.
Ⅱ.配制时,容量瓶有少量蒸馏水
Ⅲ.定容时仰视刻度线
考点:物质的量浓度的相关计算,配制一定物质的量浓度的溶液
专题:实验题
分析:(1)根据c=
计算;
(2)溶液是均匀的,溶液的密度、浓度不随体积变化;
(3)①根据稀释定律,稀释前后HCl的物质的量不变,据此计算需要浓盐酸的体积;
②利用浓盐酸稀释配制500mL稀盐酸溶液,需要的仪器有:量筒、烧杯、玻璃棒、500mL容量瓶、胶头滴管;
③分析操作对溶质物质的量、溶液体积的影响,根据c=
判断对所配溶液浓度的影响.
| 1000ρw |
| M |
(2)溶液是均匀的,溶液的密度、浓度不随体积变化;
(3)①根据稀释定律,稀释前后HCl的物质的量不变,据此计算需要浓盐酸的体积;
②利用浓盐酸稀释配制500mL稀盐酸溶液,需要的仪器有:量筒、烧杯、玻璃棒、500mL容量瓶、胶头滴管;
③分析操作对溶质物质的量、溶液体积的影响,根据c=
| n |
| V |
解答:
解:(1)质量分数36.5%、密度1.19g/mL 浓盐酸的物质的量浓度=
mol/L,
故答案为:11.9;
(2)溶液是均匀的,溶液的密度、浓度不随体积变化,而HCl的物质的量及Cl-的数目与溶液体积有关,
故答案为:BD;
(3)①令需要浓盐酸的体积为V mL,根据稀释定律,稀释前后HCl的物质的量不变,则:
V×10-3L×11.9mol/L=0.5 L×0.400mol/L
解得:V=16.8
故答案为:16.8;
②利用浓盐酸稀释配制500mL稀盐酸溶液,需要的仪器有:量筒、烧杯、玻璃棒、500mL容量瓶、胶头滴管,故还需要的仪器有:量筒、500mL容量瓶,
故答案为:量筒、500mL容量瓶;
③Ⅰ.定容后经振荡、摇匀、静置,发现液面下降,少量溶液残留在瓶口与瓶塞之间,再加适量的蒸馏水,导致溶液体积偏大,所配溶液浓度偏低;
Ⅱ.溶液配制需加水定容,配制时,容量瓶有少量蒸馏水对所配溶液浓度无影响;
Ⅲ.定容时仰视刻度线,溶液液面在刻度线上方,溶液的体积偏大,所配溶液浓度偏低,
故答案为:偏低;无影响;偏低.
| 1000×1.19×36.5% |
| 36.5 |
故答案为:11.9;
(2)溶液是均匀的,溶液的密度、浓度不随体积变化,而HCl的物质的量及Cl-的数目与溶液体积有关,
故答案为:BD;
(3)①令需要浓盐酸的体积为V mL,根据稀释定律,稀释前后HCl的物质的量不变,则:
V×10-3L×11.9mol/L=0.5 L×0.400mol/L
解得:V=16.8
故答案为:16.8;
②利用浓盐酸稀释配制500mL稀盐酸溶液,需要的仪器有:量筒、烧杯、玻璃棒、500mL容量瓶、胶头滴管,故还需要的仪器有:量筒、500mL容量瓶,
故答案为:量筒、500mL容量瓶;
③Ⅰ.定容后经振荡、摇匀、静置,发现液面下降,少量溶液残留在瓶口与瓶塞之间,再加适量的蒸馏水,导致溶液体积偏大,所配溶液浓度偏低;
Ⅱ.溶液配制需加水定容,配制时,容量瓶有少量蒸馏水对所配溶液浓度无影响;
Ⅲ.定容时仰视刻度线,溶液液面在刻度线上方,溶液的体积偏大,所配溶液浓度偏低,
故答案为:偏低;无影响;偏低.
点评:本题考查物质的量浓度计算、一定物质的量浓度溶液配制等,难度不大,注意根据c=
理解溶液配制原理及进行误差分析.
| n |
| V |

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列各组物质,前者加入后者时,无论前者是否过量,都能用同一离子方程式表示的是( )
| A、稀盐酸,Na2CO3溶液 |
| B、氯化铝溶液,氨水 |
| C、碳酸氢钠溶液,澄清石灰水 |
| D、溴化亚铁溶液,氯水 |
下列各组中的两个反应,可用同一离子方程式表示的是( )
| A、CaCO3和HCl、Na2CO3和HCl |
| B、BaCl2和H2SO4、Ba(OH)2和H2SO4 |
| C、HNO3和K2CO3、HCl和NaHCO3 |
| D、KOH和H2SO4、Ba(OH)2和HNO3 |
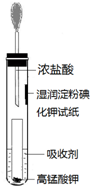 氯气是一种常用的自来水消毒剂.但是,由于氯气贮运不方便,且具有一定的危险性,目前正逐渐被其他性能优越的消毒产品所替代.请回答:
氯气是一种常用的自来水消毒剂.但是,由于氯气贮运不方便,且具有一定的危险性,目前正逐渐被其他性能优越的消毒产品所替代.请回答: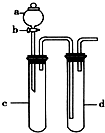 铜与稀硝酸反应产生NO,NO又被氧化成NO2,对实验观察无色NO有干扰,过多的NO、NO2又会污染环境.改进实验的设计符合绿色化学的思想.某兴趣小组设计出下图所示装置置来改进教材中“铜与硝酸反应”的实验,以探究化学实验的绿色化.
铜与稀硝酸反应产生NO,NO又被氧化成NO2,对实验观察无色NO有干扰,过多的NO、NO2又会污染环境.改进实验的设计符合绿色化学的思想.某兴趣小组设计出下图所示装置置来改进教材中“铜与硝酸反应”的实验,以探究化学实验的绿色化.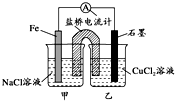 某实验小组同学对电化学原理进行了一系列探究活动.
某实验小组同学对电化学原理进行了一系列探究活动.