题目内容
下列有关物质的表达式不正确的是( )
| A、乙烯的最简式:C2H4 |
| B、CS2分子的结构式:S═C═S |
| C、醛基的结构简式:-CHO |
D、(羟基)的电子式为: |
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.乙烯的最简式中没有标出其官能团碳碳双键;
B.二硫化碳的结构式与二氧化碳类似,分子中存在两个共价键;
C.醛基中存在1个碳氢键和1个碳氧双键,为中性原子团;
D.羟基为中性原子团,存在1个氧氢键,氧原子最外层为7个电子.
B.二硫化碳的结构式与二氧化碳类似,分子中存在两个共价键;
C.醛基中存在1个碳氢键和1个碳氧双键,为中性原子团;
D.羟基为中性原子团,存在1个氧氢键,氧原子最外层为7个电子.
解答:
解:A.乙烯含有官能团碳碳双键,结构简式中必须标出官能团,乙烯正确的最简式为CH2=CH2,故A错误;
B.CS2分子中存在两个碳硫双键,其结构式为:S═C═S,故B正确;
C.醛基为醛类的官能团,醛基的结构简式为:-CHO,故C正确;
D.氧原子与氢原子通过一对共用电子对连接,羟基中的氧原子含有一个未成对电子,电子式为: ,故D正确;
,故D正确;
故选A.
B.CS2分子中存在两个碳硫双键,其结构式为:S═C═S,故B正确;
C.醛基为醛类的官能团,醛基的结构简式为:-CHO,故C正确;
D.氧原子与氢原子通过一对共用电子对连接,羟基中的氧原子含有一个未成对电子,电子式为:
 ,故D正确;
,故D正确;故选A.
点评:本题考查了结构式、结构简式、电子式等化学用语的判断,题目难度中等,注意掌握常见化学用语的概念及表示方法,明确结构简式与结构式、电子式的区别,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案
相关题目
一定量的混合气体在密闭容器中发生反应 m A (g)+n B (g)?p C (g)达到平衡后,温度不变,将气体体积缩小到原来的
,达到平衡时,C的浓度为原来的2.5倍,则下列说法不正确的是( )
| 1 |
| 2 |
| A、m+n>p |
| B、C的体积分数增加 |
| C、平衡向正反应方向移动 |
| D、A 的转化率降低 |
某溶液中仅含有Na+、Mg2+、SO42-、Cl-四种离子,其物质的量浓度比为c(Na+):c(Mg2+):c(Cl-)=3:4:5,若Na+的物质的量浓度为3mol?L-1,则SO42-的物质的量浓度为( )
| A、2 mol?L-1 |
| B、3 mol?L-1 |
| C、4 mol?L-1 |
| D、8 mol?L-1 |
在一个1L的密闭容器中,加入2molA和1molB,发生下述反应:2A(g)+B(g)?3C(g)+D(g)达到平衡时,C的浓度为1.2mol/L,C的体积分数为a%.维持容器的体积和温度不变,按下列配比作为起始物质,达到平衡后,C的浓度仍是1.2mol/L的是( )
| A、6mol C+2mol D |
| B、1mol A+0.5mol B+1.5mol C+0.5mol D |
| C、1mol A+0.5mol B+1.5mol C |
| D、4mol A+2mol B |
某位同学配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因是( )
| A、所用NaOH已经潮解 |
| B、向容量瓶中加水未到刻度线 |
| C、有少量NaOH溶液残留在烧杯里 |
| D、用带游码的托盘天平称2.4gNaOH时误用了“左码右物”方法 |
下列食品添加剂与其作用不相匹配的是( )
| A、叶绿素:着色剂 |
| B、亚硝酸钠:调味剂 |
| C、碳酸钠:疏松剂 |
| D、苯甲酸钠:防腐剂 |


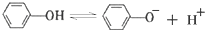 ,苯酚的酸性大于
,苯酚的酸性大于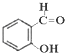 (邻羟基苯甲醛),其原因是
(邻羟基苯甲醛),其原因是