题目内容
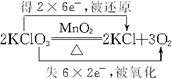
5.(1)写出下列反应的化学方程式,用双线桥标明电子转移的方向和数目,并注明“被氧化”、“被还原”.KClO3和MnO2在共热条件下反应:
 .
.(2)写出下列反应的离子方程式,并用单线桥标明电子转移的方向和数目.
实验室制Cl2的反应为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O:
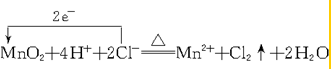 .
.
分析 (1)氯酸钾分解生成KCl和氧气,该反应中Cl元素化合价由+5价变为0价、O元素化合价由-2价变为0价,结合氧化还原反应的电子转移知识分析;
(2)MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O中,Mn元素的化合价由+4价降低到+2价,Cl元素的化合价由-1价升高到0价,结合氧化还原反应的电子转移知识分析.
解答 解:(1)氯酸钾分解生成KCl和氧气,其反应的方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,该反应中Cl元素化合价由+5价变为0价,O元素化合价由-2价变为0价,转移的电子数目为: ;故答案为:
;故答案为: ;
;
(2)MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O中,Mn元素的化合价降低,氧化剂为MnO2,MnCl2为还原产物,Cl元素的化合价升高,被氧化,HCl为还原剂,Cl2为氧化产物,则1mol氧化剂反应转移2mol2e-,改写成离子方程式以及用双线桥法表示反应中电子转移的数目为: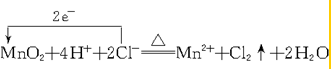 ,故答案为:
,故答案为: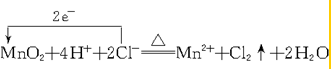 .
.
点评 本题考查氧化还原反应,把握发生的化学反应及反应中元素的化合价变化为解答的关键,侧重基本概念和转移电子的考查,题目难度不大.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
15.某水溶液中可能含有K+、Na+、Fe2+、Fe3+、Al3+、SO42-、ClO-、NO2-、SiO32-、CO32-中的若干种离子.某同学取四份该溶液各10mL进行如下实验:
①第一份加入足量稀盐酸,无任何气体和沉淀产生;
②第二份加入足量NaOH,经搅拌、过滤、洗涤、灼烧,最后得到1.6g红棕色固体;
③第三份加入酸性KMnO4溶液会使其褪色,滴至终点时共消耗0.1mol•L-1酸性KMnO4溶液10.00mL;
④第四份用洁净的铂丝做焰色反应实验,直接观察,火焰呈黄色
关于上述实验,下列说法正确的是( )
①第一份加入足量稀盐酸,无任何气体和沉淀产生;
②第二份加入足量NaOH,经搅拌、过滤、洗涤、灼烧,最后得到1.6g红棕色固体;
③第三份加入酸性KMnO4溶液会使其褪色,滴至终点时共消耗0.1mol•L-1酸性KMnO4溶液10.00mL;
④第四份用洁净的铂丝做焰色反应实验,直接观察,火焰呈黄色
关于上述实验,下列说法正确的是( )
| A. | 仅由实验②即可推断原混合溶液中一定存在Fe3+ | |
| B. | 要确定原混合溶液是否含有ClO- 至少需完成实验①②③ | |
| C. | 该溶液阳离子中一定存在Na+、Fe2+、Fe3+,一定不存在Al3+,无法确定是否含有K+ | |
| D. | 溶液中阴离子只有SO42-,且c(SO42-)大于2.75moL/L |
16.下表为元素周期表的一部分,请参照元素①-⑩在表中的位置,回答下列问题:
(1)自然界物质种类最多的元素在周期表中的位置是第二周期第IV族
(2)⑧⑨⑩的离子半径由大到小的顺序为S2->Cl->Na+(填化学用语).
(3)写出由⑥、⑧、⑩元素形成的一种离子化合物的电子式
(4)根据斜线性质相似规则,②的最高价氧化物对应的水化物与盐酸反应的离子方程式LiOH+H+=Li++H2O
(5)③的氧化物,氢氧化物有两性,写出③的单质与⑧的最高价氧化物的水化物反应的化学方程式Be+2OH-=BeO22-+H2↑
(6)已知W+X=Y+Z,W、X、Y、Z分别是由①⑤⑥三种元素形成的四种十电子粒子,写出该反应式NH4++OH-=NH3+H2O.
| IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ||
| 3 | ⑧ | ⑨ | ⑩ |
(2)⑧⑨⑩的离子半径由大到小的顺序为S2->Cl->Na+(填化学用语).
(3)写出由⑥、⑧、⑩元素形成的一种离子化合物的电子式

(4)根据斜线性质相似规则,②的最高价氧化物对应的水化物与盐酸反应的离子方程式LiOH+H+=Li++H2O
(5)③的氧化物,氢氧化物有两性,写出③的单质与⑧的最高价氧化物的水化物反应的化学方程式Be+2OH-=BeO22-+H2↑
(6)已知W+X=Y+Z,W、X、Y、Z分别是由①⑤⑥三种元素形成的四种十电子粒子,写出该反应式NH4++OH-=NH3+H2O.
20.下列离子在溶液中能大量共存的是( )
| A. | Cl-、NO3-、Fe3+、Na+ | B. | Ag+、NO3-、Cl-、K+ | ||
| C. | K+、Ba2+、OH-、SO42- | D. | Cu2+、NH4+、Br-、OH- |
10.下列离子方程式书写正确的是( )
| A. | 碳酸钙与盐酸反应:CO32-+2H+═CO2↑+H2O | |
| B. | 硫酸氢钠溶液中加入足量烧碱溶液:HSO4-+OH-═SO42-+H2O | |
| C. | Ba(OH)2与H2SO4反应到恰好沉淀完全:Ba2++OH-+SO42-+H+═BaSO4↓+H2O | |
| D. | 向澄清的石灰水中滴入少量碳酸氢钠溶液:Ca2++OH-+HCO3-═CaCO3↓+H2O |
17.下列叙述不正确的是( )
| A. | 溶质质量分数分别为a%和5a%的硫酸溶液按等体积混合,混合溶液中硫酸的质量分数大于3a% | |
| B. | 将1体积cmol/L硫酸溶液用水稀释为5体积,得到0.2cmol/L硫酸溶液 | |
| C. | 10mL质量分数14%的氨水,用水稀释至100mL,氨水的质量分数小于1.4% | |
| D. | 将w g a% NaCl溶液蒸发掉$\frac{w}{2}$ g水,得到4a% NaCl溶液 |