题目内容
14.实验室用KMnO4与密度为1.19g•cm-3,溶质质量分数为36.5%的HCl溶液反应制取氯气,反应方程式为:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O
(1)用双桥线法分析电子转移的方向和数目
(2)上述反应中氧化剂是:KMnO4;还原剂是:HCl;
(3)浓盐酸在反应中表现出来的性质是C;
A.只有还原性 B.只有氧化性 C.还原性和酸性 D.氧化性和酸性
(4)氧化产物和还原产物的质量之比是:1:5.
分析 (1)反应中高锰酸钾为氧化剂,浓盐酸为还原剂,根据Mn元素的化合价+7→+2,Cl元素的化合价-1→0,标出电子的转移方向和数目;
(2)反应中锰元素得电子,氯元素失电子;
(3)浓盐酸中Cl失电子作还原剂,生成氯化锰还表现酸性;
(4)反应中16molHCl中只有10molHCl 作还原剂.
解答 解:(1)反应中高锰酸钾为氧化剂,浓盐酸为还原剂,Mn元素的化合价+7→+2,和Cl元素的化合价-1→0,反应中氧化剂和还原剂得失电子数目相等,
即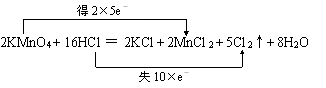 ,
,
故答案为: ;
;
(2)2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O反应中锰元素得电子,则KMnO4为氧化剂,氯元素失电子,HCl为还原剂;
故答案为:KMnO4;HCl;
(3)浓盐酸中Cl元素失电子作还原剂,表现还原性,生成氯化锰还表现酸性,所以反应中浓盐酸表现酸性和还原性;
故答案为:C;
(4)反应中16molHCl中只有10molHCl 作还原剂,则氧化产物和还原产物的质量之比是1:5;
故答案为:1:5.
点评 本题考查氧化还原反应,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意氧化还原反应中基本概念,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.只用一种试剂,可区别Na2SO4、MgSO4、FeCl2、AlCl3四种溶液,这种试剂是( )
| A. | AgNO3 | B. | BaCl2 | C. | NaOH | D. | HCl |
9.下列有关胶体的说法不正确的是( )
| A. | 向Al(OH )3胶体中加入酒精溶液能发生聚沉现象 | |
| B. | 豆浆和雾都是胶体 | |
| C. | Fe(OH )3 胶体能透过滤纸 | |
| D. | 向沸水中加入饱和的FeCl3溶液,可制备Fe(OH )3 胶体 |
19.下列变化过程,属于放热反应的是( )
①Ba(OH)2•8H2O 与NH4Cl反应 ②酸碱中和 ③浓硫酸稀释 ④固体NaOH溶于水 ⑤硫在空气或氧气中燃烧.
①Ba(OH)2•8H2O 与NH4Cl反应 ②酸碱中和 ③浓硫酸稀释 ④固体NaOH溶于水 ⑤硫在空气或氧气中燃烧.
| A. | ②③④⑤ | B. | ②③④ | C. | ②⑤ | D. | ①③⑤ |
6.青蒿素(分子式为C15H22O5)是从植物黄花蒿叶中提取的可用于治疗疟疾的药物.我国科学家屠呦呦因在青蒿素及双氢青蒿素(分子式为C15H24O5)领域的开创性研究分享了2015诺贝尔生理学及医学奖,成为了首位获得诺贝尔奖的中国本土科学家.青蒿素为无色针状晶体,味苦.在乙醚中可溶解,在水中几乎不溶.下列说法正确的是( )
| A. | 青蒿素的摩尔质量为282g | |
| B. | 青蒿素的化学合成方法没有任何研究意义 | |
| C. | 青蒿素转化为双氢青蒿素是物理变化 | |
| D. | 用乙醚提取黄花蒿叶中的青蒿素比用水效果好 |
3.若NA为阿伏加德罗常数的值,下列说法不正确的是( )
| A. | NA个Fe(OH)3胶体粒子的质量为107g | |
| B. | 8.0gCu2S和CuO的混合物中含有铜原子数为0.1NA | |
| C. | 1 molCl2与足量Fe反应转移电子数一定为2NA | |
| D. | 2.3gNa与氧气完全反应,反应中转移的电子数0.1NA |
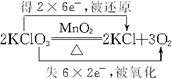 .
.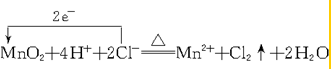 .
.